��Ŀ����
����Ŀ��ͬѧ��������ͼ��ʾװ�ý���������Ʊ�ʵ�飨A��FΪװ�ñ�ţ��� 
��1��д��ͼDװ���м����������� ��
��2����Aװ�ü�������غͶ������̵Ļ������ȡ��������ѧ����ʽΪ �� ���ж������������ã��ռ���������ѡ������װ�ñ�ţ�
��3��ʵ������ȡCO2ͨ��ѡ������ҩƷ�е�����ҩƷ��ţ�
a��ϡ���� b����ʯ�� c����״ʯ��ʯ d��ϡ����
ͨ������CO2����ķ�Ӧ���û�ѧ����ʽ��ʾΪ ��
��4�������£����ù�����������FeS����ϡ���ᷴӦ��ȡ���⣨H2S�����壬��Ҫ���Ƶμ�Һ������ʣ���ѡ��ķ���װ��������װ�ñ�ţ���ͬ����ʵ������ȡ����Ӧѡ��ķ������ռ�װ�õ���Ͽ���ʹ ��
��5����ȡ����ǰӦ�ȼ��װ�õ������ԣ�����Fͼ��ʾ����������ڵ��ܿ�δ�������ݣ������ԭ�������������ص���������ţ���
a�����ձ�����ˮ�� b����������ˮ��λ�ù���������ݳ�
c����ˮ���ɱ�ˮ d����������ס�Թܱڣ��ٽ�������һ�˲���ˮ�У�
���𰸡�
��1������ƿ
��2��2KClO3 ![]() 2KCl+3O2��������D��E
2KCl+3O2��������D��E
��3��ac��Ca��OH��2+CO2�TCaCO3��+H2O
��4��C��CE��BE
��5��abc
���������⣺��1������ʵ���ҳ���������֪�����Ǽ���ƿ����2��ʵ�����ü�������غͶ������̵Ļ������ȡװ�õ��������ڹ̹̼����͵�Aװ�ã���Ϊ�������ܶȱȿ�����������ˮ���ʿ��Բ��������ſ���������ˮ���ռ������ж���������Ϊ�����������ã���Ӧ�ķ���ʽΪ��2KClO3 ![]() 2KCl+3O2������3��ʵ������ȡ������̼���壬ʹ�õ�ҩƷ�Ǵ���ʯ��ʯ��ʯ��ϡ���ᣬ������̼��ʹ�����ʯ��ˮ����ǣ�����Ϊ������̼��ʯ��ˮ�е��������Ʒ�Ӧ������̼��Ƴ�����ˮ����Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+CO2�TCaCO3��+H2O�� ��4����ȡ����ʱ����Ҫ���ȣ���Ҫ���Ƶμ�Һ������ʣ���ѡ��ķ���װ���ǣ�Ӧ����Cװ����Ϊ����װ�ã���п��ϡ���ᷴӦ��������п����������Ӧ�Ļ�ѧ����ʽΪ��Zn+H2SO4�TZnSO4+H2������ʵ��������п��ϡ���ᷴӦ��ȡ���������ڹ�Һ�����ͣ�����Ӧ��ѡ��B��Cװ������ȡ�����������ܶȱȿ���С��������ˮ������Ӧ��ѡ��Eװ�����ռ���������5����ȡ����ǰӦ�ȼ��װ�õ������ԣ�����Fͼ��ʾ����������ڵ��ܿ�δ�������ݣ������ԭ�������������ص���
2KCl+3O2������3��ʵ������ȡ������̼���壬ʹ�õ�ҩƷ�Ǵ���ʯ��ʯ��ʯ��ϡ���ᣬ������̼��ʹ�����ʯ��ˮ����ǣ�����Ϊ������̼��ʯ��ˮ�е��������Ʒ�Ӧ������̼��Ƴ�����ˮ����Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+CO2�TCaCO3��+H2O�� ��4����ȡ����ʱ����Ҫ���ȣ���Ҫ���Ƶμ�Һ������ʣ���ѡ��ķ���װ���ǣ�Ӧ����Cװ����Ϊ����װ�ã���п��ϡ���ᷴӦ��������п����������Ӧ�Ļ�ѧ����ʽΪ��Zn+H2SO4�TZnSO4+H2������ʵ��������п��ϡ���ᷴӦ��ȡ���������ڹ�Һ�����ͣ�����Ӧ��ѡ��B��Cװ������ȡ�����������ܶȱȿ���С��������ˮ������Ӧ��ѡ��Eװ�����ռ���������5����ȡ����ǰӦ�ȼ��װ�õ������ԣ�����Fͼ��ʾ����������ڵ��ܿ�δ�������ݣ������ԭ�������������ص���
���ձ�����ˮ�ۣ���������ˮ��λ�ù���������ݳ�����ˮ���ɱ�ˮ �أ�
����ʱӦ�Ƚ����ܷ���ˮ�У���������ס�Թܱڣ���d�йأ�
�𰸣���1������ƿ����2��2KClO3 ![]() 2KCl+3O2��������D��E����3��ac��Ca��OH��2+CO2�TCaCO3��+H2O����4��C��CE��BE����5��abc
2KCl+3O2��������D��E����3��ac��Ca��OH��2+CO2�TCaCO3��+H2O����4��C��CE��BE����5��abc
�����㾫����������Ŀ����֪���������ô������ص�������úͶ�����̼�ļ�������������֪ʶ���Եõ�����Ĵ𰸣���Ҫ���մ�������ý�����ڻ�ѧ��Ӧ���ܸı��������ʵĻ�ѧ��Ӧ���ʣ��������������ͻ�ѧ�����ڷ�Ӧǰ��û�з����仯�����ʣ���һ�������䣩�����ڻ�ѧ��Ӧ����������ýд����ã���֤���������Ƶõ�����ͨ������ʯ��ˮ�����ܻ��ǣ����Ƕ�����̼�������������õ�ȼ��ľ�������ڼ���ƿ�ڣ�ľ��Ϩ��֤���Ѽ���������̼���壮

����Ŀ��̽��Ӱ�컯ѧ��Ӧ���ʵ�����
��1�����ֺ��������
þ�ڿ������ܹ�����ȼ�գ���˿���������ܹ�����ȼ�գ�������»�������˵����������֮���ܷ�����Ӧ�Լ���Ӧ���ʵ������� ��
������������ȼ�ձ��ڿ�����ȼ�վ��ң���һ������Ӱ�컯ѧ��Ӧ���ʵ������������죬��ʳƷ���ڱ����ﲻ���ױ��ʣ���һ����˵���¶�Ҳ��Ӱ�컯ѧ��Ӧ���ʣ��¶����Ӱ�췴Ӧ�����أ�
��2�����������
�¶�Խ�ߣ���Ӧ����Խ��
�ռ�֤��
ʵ��ҩƷ��������С��ͬ��п����������ͬ����������������ͬ�¶ȵ�ϡ���ᣨ20�桢40�棩
��ѡ������ҩ�ס����巢��װ��2�ף����������ã�����Ͳ2֧����Һ©�����������ͷ�ιܡ�ˮ�ۡ����Թ�2֧����������������ҩƷ����������±���ʵ�鱨�森
�۲��������� | ѡ�õ����� | ʵ�鲽�� | ʵ������ | ʵ����� |
������ͬ�����һ�Թܣ�����������ʱ�� | ���巢��װ�á��������ͷ�ιܡ�ˮ�ۡ����Թܡ� | �¶�Խ�ߣ���Ӧ����Խ�죮��Ӧ�Ļ�ѧ����ʽ�� |
��ʵ����Թ۲����������ж��֣����������۲���⣬���Թ۲������������У�дһ���� ��
��3�����������
���۵ĽǶȷ������¶�Խ�ߣ���Ӧ����Խ�족��ԭ���� ��
��4����չ����
���������ⶨ��λ��ʵ��С���ͬѧ������п����ϡ���ᷴӦ����������������ʱ��仯�����ߣ���ͼ��ʾ�����ͼ������ʱ��0��t�ڣ���Ӧ�����ӿ����Ҫԭ���� �� ʱ��t�Ժ�Ӧ������������Ҫԭ���� �� 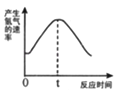
����Ŀ����ͬѧΪ�������������ƺ�����������Һ���������ͼ��ʾ������ʵ�鷽���� 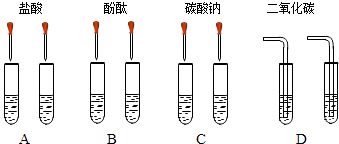
��1�������ܴﵽʵ��Ŀ����
��2����C��ʵ���з����Ļ�ѧ����ʽΪ
��3��ʵ�������ͬѧ��A��C����֧�Թ��е���Һ����ͬһ�����У�������Һ����ǣ�������˵�����������ɣ��ѧʽ���������̪����Һ�ʺ�ɫ��
��4�������̪����Һ�ʺ�ɫ��˵����Һ�ʼ��ԣ�ʹ��Һ�ʼ��Ե�������ʲô�أ���ͬѧ��һ���Ʋ⣺��Һ�гʼ��Ե����ʿ�����̼���ơ��������ƺ����������е�һ�֣����������������������ɵĻ���
��5��Ϊ����֤�Ʋ⣬��ͬѧ�������ϣ���Ϥ�Ȼ�����Һ�����ԣ����������ʵ�������֤�������Ҫ��������пհף�
ʵ������ | Ԥ������ | ���� |
ȡ���������е��ϲ���Һ���Թ��У�����������Ȼ�����Һ������ | �����а�ɫ��������Һ����ɫ | ������̼���� |
�����������ɣ���Һ�ʺ�ɫ | �������������� | |
�����а�ɫ��������Һ�ʺ�ɫ |
��6����ͬѧ��Ϊ��ͬѧ�ڢڲ���֤�Ľ��۲����ܣ�ԭ���� ��