题目内容
【题目】通过过滤操作除去了粗盐中的难溶性杂质,还含有 CaCl2、Na2SO4、MgCl2 等可溶性杂质。如图:
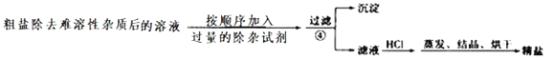
按顺序加入过量的下列除杂试剂后,过滤。在滤液中加入过量盐酸蒸发,即可得到纯净的氯化钠。除杂试剂及顺序可行的是______________。
A BaCl2、NaOH、Na2CO3 B Ba(OH)2 、Na2CO3 C Na2CO3、BaCl2、NaOH
【答案】AB
【解析】
A、加入氯化钡可以和硫酸钠生成硫酸钡沉淀和氯化钠用以去除硫酸钠,加入氢氧化钠可以和氯化镁生成氢氧化镁沉淀和氯化钠,去除氯化镁,加入碳酸钠可以和氯化钙反应生成碳酸钙沉淀和氯化钠,可以和过量的氯化钡生成碳酸钡沉淀和氯化钠,过滤之后滤液中只剩下氯化钠、碳酸钠、氢氧化钠,滤液加盐酸可以去除过量的氢氧化钠和碳酸钠生成氯化钠和水,最终只得到氯化钠,故A符合题意;
B、首先加入氢氧化钡可以去除氯化镁生成氢氧化镁沉淀和氯化钡,可以去除硫酸钠生成硫酸钡沉淀和氢氧化钠,然后加入碳酸钠可以去除氯化钙和第一步生成的氯化钡生成碳酸钙沉淀、碳酸钡沉淀和氯化钠,最后过滤,过滤之后滤液中只剩下氯化钠、碳酸钠、氢氧化钠,滤液加盐酸可以去除过量的氢氧化钠和碳酸钠生成氯化钠和水,最终只得到氯化钠,故B符合题意;
C、首先加入碳酸钠可以去除氯化钙生成碳酸钙沉淀和氯化钠,然后加入氯化钡可以去除硫酸钠生成硫酸钡沉淀和氯化钠,最后加入氢氧化钠可以去除氯化镁生成氢氧化镁沉淀和氯化钠,过滤之后滤液中会氯化钠、过量氯化钡、氢氧化钠,滤液中的氯化钡在后续的操作加稀盐酸不能去除,故C不符合题意;
故选:AB

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如表所示。根据表中信息判断下列说法正确的是
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量 | 2 | 30 | 20 | 10 |
反应后的质量 | m | 39 | 5 | 16 |
A.该反应是化合反应B.甲一定是该反应的催化剂
C.反应过程中乙、丙变化的质量比为3:5D.丙可能是单质
【题目】在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:下列说法正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量(g) | 24.5 | 5 | 0.1 | 0.4 |
反应后的质量(g) | 0 | 5 | 15 | x |
A.乙是反应物B.x=10C.该反应为化合反应D.丁是催化剂