题目内容
【题目】某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了右图实验,对固体B的成分进行了分析和实验探究.
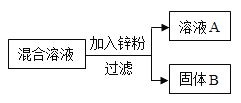
(提出问题)固体B中的成分可能有哪些?
(作出猜想)甲同学:只有Ag
乙同学:Zn、Ag
丙同学:Cu、Ag
请写出你的一种猜想(1)______
(表达交流)写出甲同学猜想的理由(2)______
(反思评价)请你评价乙同学的猜想(3)______
(实验探究)想证明自己的猜想正确
实验步骤 | 现象 | 由此确定固体B的成分写出反应的化学方程式 |
取少量固体B,滴加(4)______ | 有气泡产生 | (5)______ |
在得出固体B的成分后,也确定了液体A的成分,液体A中含有的物质有(化学式)(6)______.
【答案】Ag、Cu、Zn 当AgNO3有剩余时,锌和硝酸银反应生成银和硝酸锌,固体B成分只有Ag或锌和硝酸银刚好完全反应,固体B成分只有Ag 不合理,Zn应先与AgNO3反应后与Cu(NO3)2反应 稀盐酸(或稀硫酸等) ![]() (或
(或![]() ) Zn(NO3)2
) Zn(NO3)2
【解析】
由金属活动性顺序及其运用可知,向AgNO3和Cu(NO3)2混合溶液中加入锌粉,Zn应先与AgNO3反应后与Cu(NO3)2反应.由于锌粉量的不同,溶液A中的溶质不同.当锌的量过量时,溶液中的溶质只有Zn(NO3)2,固体为:Ag、Cu、Zn;当锌的量过量时,溶液中的溶质只有Zn(NO3)2或当AgNO3有剩余时,溶液中的溶质是:Zn(NO3)2、AgNO3、Cu(NO3)2,固体为:只有Ag。
[作出猜想]实验要做对比,甲同学:只有Ag、乙同学:Zn、Ag、丙同学:Cu、Ag
故猜想:Ag、Cu、Zn
[表达交流]甲同学猜想的理由:当AgNO3有剩余时,锌和硝酸银反应生成银和硝酸锌,固体B成分只有Ag或锌和硝酸银刚好完全反应,固体B成分只有Ag。
[反思评价]乙同学的猜想不合理;理由是:Zn应先与AgNO3反应后与Cu(NO3)2反应。
[实验探究]当锌粉过量时,溶液中的溶质只有Zn(NO3)2,固体B中有锌,当加入酸时有气泡生成。
实验步骤 | 现象 | 有关反应的化学方程式 |
稀盐酸(或稀硫酸等) | 有气泡产生 |
|
在得出固体B的成分后,也确定了液体A的成分,由于锌的量过量,溶液中的溶质只有Zn(NO3)2。

【题目】化学实验是学习化学的基础,请根据下列装置图回答问题。
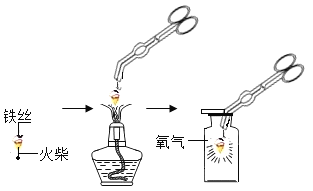
(1)铁丝绕成螺旋状的原因是___________。
(2)小明按图示进行实验时,集气瓶炸裂了,其可能的原因是___________。
(3)图中螺旋状铁丝的末端系一根火柴的作用是_____。
(4)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4 mm)放入氧气中燃烧时的实验现象的记录。请你分析后回答问题:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | (未填) |
①你认为表中未填完整的实验现象是__________________。
②造成铁丝在氧气中燃烧时火星四射的主要原因是_______________。