题目内容
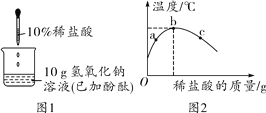
【题目】取盐酸与氯化铜的混合溶液54g放入烧杯中,逐滴滴入质量分数为20%的NaOH溶液,产生沉淀质量与滴入NaOH溶液质量的关系如图所示.
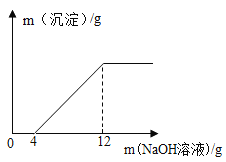
(1)滴入NaOH溶液的质量在0~4g时,NaOH与_______反应;
(2)原盐酸与氯化铜的混合溶液中氯化铜的质量分数_______(写出计算过程).
【答案】盐酸 5%
【解析】
(1)由于是盐酸和氯化铜的混合溶液,加入氢氧化钠时,由于氢氧化铜能够和盐酸反应,所以盐酸先和氢氧化钠反应,待盐酸完全反应后,氯化铜和氢氧化钠反应。滴入氢氧化钠溶液的质量在0~4g时,氢氧化钠与盐酸反应。
(2)设原盐酸与氯化铜混合溶液中氯化铜的质量分数为x。
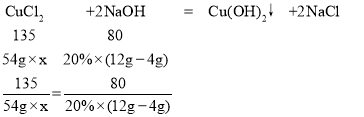
解得:x=5%
答:(1)滴入氢氧化钠溶液的质量在0~4g时,氢氧化钠与盐酸反应。
(2)原盐酸与氯化铜混合溶液中氯化铜的质量分数为5%。

 通城学典默写能手系列答案
通城学典默写能手系列答案【题目】硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
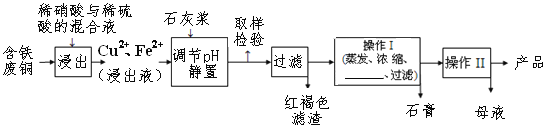
胆矾和石膏在不同温度下的溶解度(g/100g水)如表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是____________;
(2)石灰浆调pH大约要调节到__________
A. 2 B. 5 C. 7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式________________________________;
(4)操作I最后温度应该控制在___________℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、__________、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是_________________。
【题目】某化学兴趣小组在课外活动中,为了不使实验中废水对环境造成污染,对废水进行了多次检测,其中三次检测结果如下表所示,请回答:
检测次数 | 溶液中检测出的物质 |
第一次 |
|
第二次 |
|
第三次 |
|
(1)三次检测结果中第______次检测结果不正确。
(2)由于废水中含有某些金属离子会对环境造成污染,兴趣小组的同学提出建议:用一种含钠离子的化合物、用适当的比例来处理废水,就可以同时除去废水中所有的有害金属离子。这种化合物是______。