题目内容
【题目】称取一定质量的氯酸钾和二氧化锰的混合物,放入大试管中加热至质量不再变化为止。实验测得固体混合物的质量随加热时间变化的相关数据如图所示。请计算: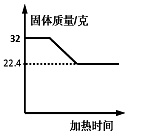
(1)生成氧气多少克?
(2)原混合物中氯酸钾的质量分数为多少?(写出计算过程,计算结果保留一位小数)
【答案】
(1)解:根据质量守恒定律知道生成氧气的质量=32克-22.4克=9.6克
(2)解:设生成9.6g氧气,需要氯酸钾的质量为x
2KClO3 | 3O2↑ |
245 | 96 |
x | 9.6g |
列比利式得:245:X=96:9.6克,解得X=24.5克
原混合物中氯酸钾的质量分数为24.5g/32gx100%=76.6%
【解析】根据质量守恒定律分析,有气体生成的反应,反应前后物质减少的质量即为生成气体的质量;根据化学方程式计算分析,利用方程式进行计算时,要先写出有关反应方程式,根据方程式量的关系找出相关物质的相对质量比,再从题中找出已知物质的质量,利用相对质量比与实际质量比相等利出比例式求解。

【题目】某同学做实验时发现,盛放NaOH溶液的瓶口与橡皮塞上,常有白色粉末出现.为探究这种白色粉末的成分,设计了如下实验.请你完成实验报告.
实验步骤 | 实验现象 | 结论和反应的化学方程式 |
1)、 | 白色粉末溶于水,形成无色溶液. | / |
2)、 | 酚酞变红. | 溶液呈碱性,含有离子. |
3)、 | 溶液由红色变为无色,并有气泡产生.产生的气体能使燃着的木条熄灭. | 溶液中含有 . |
该实验证明氢氧化钠已经变质,有关方程式 .
【题目】物质的组成结构决定性质是化学基本思想。下列说法不正确的是
A | 生铁和钢机械性能不同 | 含碳量不同 |
B | 氧气和液氧颜色不同 | 氧分子之间的间隔不同 |
C | 金刚石和石墨物理性质不同 | 碳原子的排列方式不同 |
D | 食盐在人体中能生成胃酸 | 食盐中有钠离子缘故 |
A.AB.BC.CD.D