题目内容
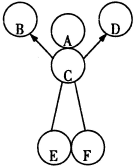
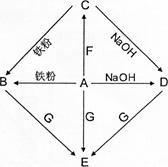
(7分)A—G是初中化学常见物质。其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀。下图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(1)请写出化学式:A ,F 。
(2)写出D→E的化学方程式:
。
(3)在A→E的反应过程中,A与G溶液恰好完全反应,反应后所得溶液的pH 7(填“>”、“=”或“<”)。
(4)C溶液与铁粉反应后,取剩余固体加入盐酸,没有气体放出。请分析:C与铁粉反应后的溶液组成中除了H2O外,一定存在的物质有 ,可能存在的物质有 。

(1)请写出化学式:A ,F 。
(2)写出D→E的化学方程式:
。
(3)在A→E的反应过程中,A与G溶液恰好完全反应,反应后所得溶液的pH 7(填“>”、“=”或“<”)。
(4)C溶液与铁粉反应后,取剩余固体加入盐酸,没有气体放出。请分析:C与铁粉反应后的溶液组成中除了H2O外,一定存在的物质有 ,可能存在的物质有 。
(1)HCl CuO(或Cu(OH)2) (2)NaCl+ AgNO3=AgCl↓+ NaNO3(3)< (4)FeCl2 CuCl2
试题分析: A的浓溶液能挥发出刺激性气味的气体,且A可与铁粉、氢氧化钠发生反应;所以A为盐酸。C→D的反应过程中有蓝色沉淀生成,且为C和氢氧化钠反应,所以沉淀为氢氧化铜,C中含铜离子。由于C是盐酸和F反应,所以C为氯化铜,则F为氧化铜或氢氧化铜。D可由盐酸、氯化铜分别和氢氧化钠反应生成,所以D为氯化钠。E为白色沉淀,且可由盐酸和氯化钠钠分别与G反应生成,所以E为氯化银,G为硝酸银。B为盐酸和铁反应生成,所以B为氯化亚铁。
(1)A为盐酸,化学式为HCl。F为氧化铜(或氢氧化铜),化学式为CuO(或Cu(OH)2)
(2)D→E的反应即为氯化钠与硝酸银反生成氯化银,反应的化学方程式为:NaCl+ AgNO3=AgCl↓+ NaNO3。
(3)在A→E的反应为盐酸和硝酸银反应生成氯化银和硝酸,所以二者恰好完全反应,反应后所得溶液为硝酸的溶液。硝酸溶液呈酸性,其pH<。
(4)C溶液为氯化铜溶液,与铁粉反应后可生成铜和氯化亚铁。“取剩余固体加入盐酸,没有气体放出”说明固体中没有铁。因此二者的反应可能是:1、铁粉量不足,则所得溶液中除了H20外,还含氯化亚铁和氯化铜。2、铁粉与硫酸铜恰好完全反应,则所得溶液为氯化亚铁溶液。所以反应后的溶液组成中除了H20外,一定存在的物质有FeCl2,可能存在的物质有CuCl2。

练习册系列答案
相关题目