题目内容
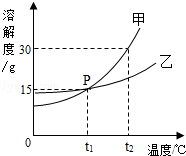
根据图A、B、C三种固体的溶解度曲线回答: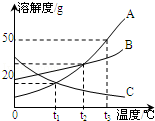
(1)在某一温度时,A、B两饱和溶液的溶质质量分数相等,此时为 ℃。
(2)在t1℃~t2℃范围内,A、B、C三种物质的溶解度由大到小的顺序为 。
(3)要使C的饱和溶液变为不饱和溶液,可采用的一种方法是 。
(4)要从含有少量A的B溶液中得到较多的B晶体,通常采用的方法是 。
(5)t3℃时,将30gA加入到装有50g水的烧杯中,充分搅拌,所得溶液的溶质质量分数为 (结果精确至0.1%)。
(6)在室温时将A物质加入到盛水的烧杯中,充分搅拌后发现仍有少量A未溶解,但放置一段时间后,发现A完全溶解了,可能的原因是 。
(1)t2;(2)B>A>C; (3)降低温度(或加水等); (4)蒸发结晶;(5)33.3%;
(6)A的晶体溶于水时吸收热量
解析试题分析:(1)根据溶解度曲线交点的意义分析。由A、B的溶解度曲线可知,在t2℃时,两条曲线交与一点,它们的溶解度相同,A、B两饱和溶液的溶质质量分数相等;
(2)根据溶解度曲线,比较溶解度的大小。由A、B、C三种固体的溶解度曲线可知,在在t1℃~t2℃范围内,A、B、C三种物质的溶解度由大到小的顺序为B>A>C;
(3)根据C的溶解度曲线随温度变化的情况分析将饱和溶液变为不饱和溶液的措施。由于C的溶解地随温度的升高而减小,所以,要使C的饱和溶液变为不饱和溶液,可采用的一种方法是:降低温度(或加水等);
(4)根据A、B的溶解度曲线随温度变化的情况分析分离混合物的方法。由A、B的溶解度曲线可知,由于A的溶解度随温度的升高而明显增大,B的溶解度随温度的升高而变化不大,要从含有少量A的B溶液中得到较多的B晶体,通常采用的方法是蒸发结晶;
(5)根据溶解度进行有关的计算。由A的溶解度曲线可知,在t3℃时,A的溶解度是50g,由溶解度的含义可知,在50g的水中只能溶解25gA物质,所得溶液的溶质质量分数为: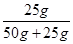 ×100%=33.3%;
×100%=33.3%;
(6)根据溶解的过程中吸热和放热的现象分析。在室温时将A物质加入到盛水的烧杯中,充分搅拌后发现仍有少量A未溶解,但放置一段时间后,发现A完全溶解了,可能的原因是A的晶体溶于水时吸收热量。
考点:考查固体溶解度曲线及其作用;结晶的原理、方法及其应用;饱和溶液和不饱和溶液相互转变的方法

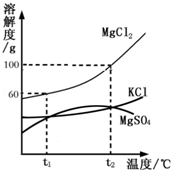
如图是甲、乙两种固体物质的溶解度曲线.
(1)在t1℃时,甲、乙两种固体物质的溶解度 (填相等或不相等);
(2)把甲物质的不饱和溶液变成饱和溶液,下列有关说法正确的是 (填字毋序号);
| A.溶剂的质量一定变小 |
| B.溶质的质量一定不变 |
| C.溶质的质量分数一定变大 |
| D.溶液的质量可能不变 |
(3)在实验室中,用固体物质甲和水配制成一定溶质质量分数的溶液,需用到的仪器有:托盘天平、烧杯、药匙、胶头滴管和 .
下图是甲、乙两种固体物质的溶解度曲线。
(1)在t1℃时,甲、乙两种固体物质的溶解度 (填相等或不相等);
(2)把甲物质的不饱和溶液变成饱和溶液,下列有关说法正确的是 (填字母序号);
| A.溶剂的质量一定变小 |
| B.溶质的质量一定不变 |
| C.该饱和溶液还可以溶解其他物质 |
| D.溶液的质量可能不变 |
苯酚是医院常用的消毒剂,其试剂瓶的标签如图。有关信息解读不正确的是:
| A.苯酚是由碳、氢、氧三种元素组成的有机物 |
| B.苯酚由碳原子、氢原子、氧原子构成 |
| C.使用苯酚需注意防止触及皮肤 |
| D.苯酚受热易熔化 |