题目内容
【题目】某工厂在生产过程中会产生大量氧化铜废料(杂质与稀硫酸不发生反应且不溶于水),工厂技术科设计如下的生产流程来回收金属,其流程图如下: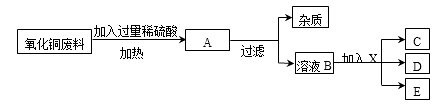
试回答下列有关问题:
(1)在加热条件下,氧化铜能与稀硫酸迅速反应生成硫酸铜和一种氧化物,该氧化物是相对分子质量最小的氧化物。则氧化铜与稀硫酸反应的化学方程式为;
(2)过滤时用到的玻璃仪器有玻璃棒、烧杯和;
(3)溶液B中的溶质为:;
(4)若D是一种浅绿色溶液,C是一种最轻的气体,则X的化学式为 , 在溶液B中加入X时发生的化学反应方程式为
【答案】
(1)![]()
(2)漏斗
(3)![]() 和
和 ![]()
(4)![]() ,
,![]() ,
,![]()
【解析】(1)相对分子质量最小的氧化物是水,则氧化铜与硫酸反应生成物为硫酸铜和水;(2)过滤要用到的仪器为烧杯、漏斗、玻璃棒、铁架台,其中铁架台不是玻璃仪器;(3)溶液B中溶质除生成的硫酸铜外,还有剩余的硫酸;(4)D是一种浅绿色溶液,则为亚铁离子溶液,C为最轻气体,即为氢气,则X为铁,在溶液B中加入铁时铁与硫酸铜溶液和硫酸溶液都发生反应。
【考点精析】解答此题的关键在于理解过滤操作的注意事项的相关知识,掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损,以及对金属材料的选择依据的理解,了解黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属.

【题目】两化学兴趣小组测定某石灰石样品中碳酸钙的质量分数(假定:石灰石样品中除碳酸钙外,其余物质不与稀盐酸反应也不溶于水;且为了反应充分,尽可能的将石灰石样品粉碎).不同的小组采用了不同的方法,但是他们都成功的测定了所取样品中碳酸钙的质量分数.
(1)【第一组】①称取12g样品放入烧杯;
②加入足量的稀盐酸至不再产生气体时,过滤、洗涤、干燥后称量剩余固体质量为3.6g;
③根据剩余固体的质量求出样品中碳酸钙的质量分数为。
(2)【第二组】①称取6g样品:按规范操作,用托盘天平称取6g样品时,若指针略向左偏转,要使指针居中的恰当操作是:;把称取好的样品放入烧杯中(烧杯质量为10g).
②将50g稀盐酸分5次加入,每次加入稀盐酸后,用玻璃棒不断搅拌,搅拌的目的是 , 然后对烧杯(包括溶液和残余固体)进行了称量,记录如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的总质量(g) | 10 | 20 | 30 | 40 | 50 |
烧杯和药品总质量(g) | 25.56 | 35.12 | 44.68 | 54.24 | 64.24 |
(3)分析数据,进行计算①样品完全反应后生成二氧化碳的质量为g.
②石灰石样品中碳酸钙的质量分数是多少?(计算结果精确到0.1 %)
③最后所得溶液的质量为g.