题目内容
【题目】请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:
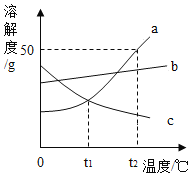
⑴在____℃时,a、c两种物质的溶解度相等。
⑵在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为______g。
⑶若a物质中混有少量b物质,最好采用______(填“降温结晶”或“蒸发结晶”)的方法提纯a。
⑷t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是_______。
⑸下列说法正确的是______(填字母)。
A 将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B 将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小
C 配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高
D t2℃时,将a物质10%的溶液蒸发溶剂质量为溶液质量一半,质量分数变为20%
【答案】t1 75 降温结晶 c>b>a BCD
【解析】
(1)在t1℃时,a、c两种物质的溶解度相等,因为该温度下它们有交点;故答案为:t1;
(2)在t2℃时,a物质的溶解度是50g,向盛有50ga物质的烧杯中加入50g水,只有25g的a物质溶解,充分溶解后,所得溶液的质量=25g+50g=75g;故答案为:75;
(3)若a物质中混有少量b物质,最好采用降温结晶的方法提纯,因为a的溶解度受温度的影响变化比b大;故答案为:降温结晶;
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是c>b>a,因为该温度下的溶解度a>b>c;故答案为:c>b>a;
(5)A、将a物质的饱和溶液变为不饱和溶液的方法由升高温度或增加溶剂,故溶质的质量分数不一定减少,故A错误;
B、升温后c有固体析出,将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小,故B正确;
C、配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则量取到水的实际体积偏少,配制的b溶液中溶质的质量分数将偏高,故C正确;
D、t2℃时,将a物质10%的溶液蒸发溶剂质量为溶液质量一半,设,溶液的质量为100份,则溶质的质量为10份,将a物质10%的溶液蒸发溶剂质量为溶液质量一半后,溶液的质量减少一半,故质量分数变为20%,故D正确。故选BCD。