题目内容
【题目】下图是实验室制取并验证某种气体化学性质的有关装置,据此回答下列问题:

(1)实验室制取O2和CO2都可选用的发生装置是__________(填字母序号),写出用此装置制取O2的化学方程式________________,如用C装置收集O2,验满方法是_______。
(2)某兴趣小组的同学将所选发生装置与E、F装置连接进行实验,若实验时F装置中澄清石灰水变浑浊,写出F装置中反应的化学方程式______________,此实验能否说明发生装置中产生的是二氧化碳气体,原因是______________。
(3)连接D、G装置可用来收集一定体积的CO2并测量生成的CO2体积,导管口_______(填“e”或“f”)应与“J ”相连接,图中植物油的作用是__________。
【答案】A  将带火星的木条放在d导管口,如复燃,则集满
将带火星的木条放在d导管口,如复燃,则集满 ![]() 不能,因为蜡烛燃烧产生二氧化碳,能使澄清石灰水变浑浊 f 防止二氧化碳溶于水
不能,因为蜡烛燃烧产生二氧化碳,能使澄清石灰水变浑浊 f 防止二氧化碳溶于水
【解析】
(1)实验室制取O2和CO2都可选用的固、液发生装置是A,此装置用过氧化氢与二氧化锰混产生水和氧气,反应的化学方程式 ,氧气的密度大于空气,如用万能瓶C装置收集O2,氧气应从c端通入,若d端处有氧气,则说明氧气已集满,氧气具有助燃性,能使带火星的木条复燃。验满方法是:将带火星的木条放在d导管口,如复燃,则集满;
,氧气的密度大于空气,如用万能瓶C装置收集O2,氧气应从c端通入,若d端处有氧气,则说明氧气已集满,氧气具有助燃性,能使带火星的木条复燃。验满方法是:将带火星的木条放在d导管口,如复燃,则集满;
(2)某兴趣小组的同学将所选发生装置与E、F装置连接进行实验,若实验时F装置中澄清石灰水变浑浊,F装置中氢氧化钙与二氧化碳反应产生碳酸钙沉淀和水的化学方程式![]() ,此实验不能说明发生装置中产生的是二氧化碳气体,原因是:蜡烛燃烧产生二氧化碳,也能使澄清石灰水变浑浊;
,此实验不能说明发生装置中产生的是二氧化碳气体,原因是:蜡烛燃烧产生二氧化碳,也能使澄清石灰水变浑浊;
(3)连接D、G装置可用来收集一定体积的CO2并测量生成的CO2体积,二氧化碳应该“短管进”装置装置内压强变大,将水从“长管”压入量筒中,导管口f应与“J ”相连接,图中植物油的作用是:防止二氧化碳溶于水,或与二氧化碳反应;

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案【题目】某些铜制品在空气中久置。表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
[查阅资料]①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
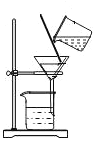
[进行实验]小组同学从铜器上取下适量的干燥铜锈,按如图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。

[解释与结论](1)依据以上现象分析,铜锈中一定含有的元素: Cu、O、_____
II.探究铜生锈的条件
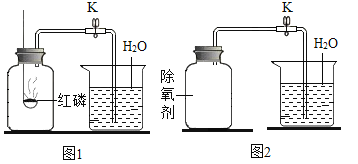
[提出猜想]根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
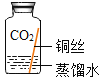
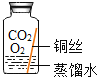
[进行实验]实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
[解释与结论]
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,请在图中将实验⑤补充完整。补充的物质应为_____。
(5)由上述实验可推知,铜生锈的条件是_____。
【题目】某实验小组的同学为了测定实验室中高锰酸钾样品的纯度,取20g该样品,依次加热该混合物,t1、t2、t3、t4时间后,称得剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 19.88 | 19.56 | 19.36 | 19.36 |
试计算:(1)加热__________时间后高锰酸钾已经完全反应。
(2)完全反应后产生氧气的质量为_________g。
(3)求该样品中高锰酸钾的质量分数_______。