题目内容
元素周期表和化学用语都是学习化学的重要工具.回答下列问题:
(1)同一周期中,相邻两种元素的质子数之差为
(2)6-11号元素中稀有气体元素的符号是 ,此表中和它化学性质相似的是
(3)硫原子的结构示意图为 ,它在反应中易 (填“得到”或“失去”)电子,它和钠元素形成的化合物的化学式为
,它在反应中易 (填“得到”或“失去”)电子,它和钠元素形成的化合物的化学式为
(4)12号元素单质在空气中燃烧时生成一种白色固体和一种黑色固体单质,则该反应的化学方程式为 .
| 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18Ar 氩 |
(2)6-11号元素中稀有气体元素的符号是
(3)硫原子的结构示意图为
 ,它在反应中易
,它在反应中易(4)12号元素单质在空气中燃烧时生成一种白色固体和一种黑色固体单质,则该反应的化学方程式为
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)根据在元素周期表中,同一周期元素从左到右原子序数依次递增的规律,进行解答;
(2)根据元素周期表解答,根据最外层电子数决定元素的性质解答;
根据镁原子结构示意图分析;根据钠原子易失去一个电子成为钠离子分析;
(3)一般来说非金属元素的原子最外层电子数等于或多于4个,在化学反应中容易得到电子,可以据此来解答该题;
(4)根据镁条在氧气中燃烧生成氧化镁,写出反应的化学方程式.
(2)根据元素周期表解答,根据最外层电子数决定元素的性质解答;
根据镁原子结构示意图分析;根据钠原子易失去一个电子成为钠离子分析;
(3)一般来说非金属元素的原子最外层电子数等于或多于4个,在化学反应中容易得到电子,可以据此来解答该题;
(4)根据镁条在氧气中燃烧生成氧化镁,写出反应的化学方程式.
解答:解:
(1)在元素周期表中,同一周期元素从左到右原子序数依次递增的规律,可得:同一周期中,相邻两种元素的质子数之差为:1.
(2)6-11号元素中稀有气体元素的符号是Ne,最外层电子数为8,由于最外层电子数决定元素的性质,Ar的最外层电子数与Ne的最外层电子数相同;
(3)由表中的原子结构示意图可知,硫原子最外层上有6个电子,大于4个,在化学反应中镁原子易得到电子成为Mg2+,钠元素的化合价为-1价,根据化合物中正负化合价的代数和为零,它和钠元素形成的化合物的化学式为Na2S;
(4)12号元素是镁元素,镁条在氧气中燃烧生成氧化镁,反应的化学方程式为:2Mg+O2
2MgO;
答案:
(1)1
(2)Ne Ar
(3)易得 Na2S
(4)2Mg+O2
2MgO
(1)在元素周期表中,同一周期元素从左到右原子序数依次递增的规律,可得:同一周期中,相邻两种元素的质子数之差为:1.
(2)6-11号元素中稀有气体元素的符号是Ne,最外层电子数为8,由于最外层电子数决定元素的性质,Ar的最外层电子数与Ne的最外层电子数相同;
(3)由表中的原子结构示意图可知,硫原子最外层上有6个电子,大于4个,在化学反应中镁原子易得到电子成为Mg2+,钠元素的化合价为-1价,根据化合物中正负化合价的代数和为零,它和钠元素形成的化合物的化学式为Na2S;
(4)12号元素是镁元素,镁条在氧气中燃烧生成氧化镁,反应的化学方程式为:2Mg+O2
| ||
答案:
(1)1
(2)Ne Ar
(3)易得 Na2S
(4)2Mg+O2
| ||
点评:本题难度不大,考查学生灵活运用元素周期表中元素的信息等进行分析解题的能力.

练习册系列答案
相关题目
在密闭的容器中加热蔗糖产生炭黑和水,这一实验说明了( )
| A、蔗糖是炭黑和水组成的纯净物 |
| B、蔗糖是炭黑和水组成的混合物 |
| C、蔗糖分子是由碳元素和水分子构成的 |
| D、蔗糖是由碳元素、氢元素和氧元素组成的 |

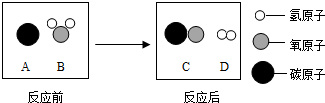

 ”表示氯原子.右图是氢气在氯气中燃烧生成氯化氢过程的微观示意图,根据图中提供的信息回答:
”表示氯原子.右图是氢气在氯气中燃烧生成氯化氢过程的微观示意图,根据图中提供的信息回答: