题目内容
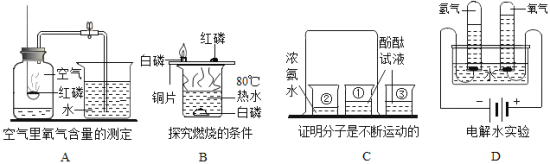
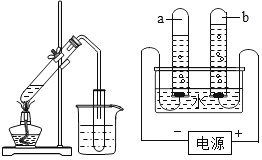
【题目】Ⅰ请根据图1中实验装置回答下列问题。
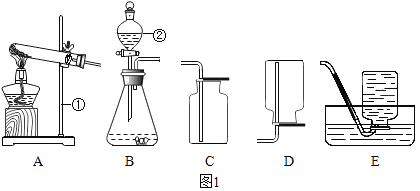
(1)写出标号仪器的名称:①_____,②_____。
(2)用高锰酸钾制取氧气,应选用的发生装置是_____。装置中反应的文字表达式为_____;选用E装置收集氧气时,判断集气瓶中已集满氧气的方法是_____。
(3)实验室也可以用装置B制取氧气,锥形瓶内放入的固体物质通常是_____,该物质在实验中起_____作用,有关反应的文字表达式为_____。写出利用该装置制取氧气的一个优点:_____。
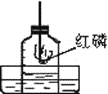
Ⅱ为探究催化剂对过氧化氢分解的催化效果,某研究小组做了如图2所示的两个实验。
(实验一)
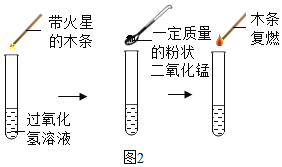
(实验二)数据记录表
1%过氧化氢溶液/mL | 50 | 50 | 50 |
加入二氧化锰的质量/g | 0.1 | 0.2 | 0.4 |
测量40s内得到氧气的体积/mL |
根据上述内容回答:
(4)你认为实验一的实验_____(填“能”或“不能”)证明二氧化锰是过氧化氢分解反应的催化剂,理由是_____。
(5)从研究小组为实验二设计的从表格内容可以看出,开展实验二的目的是_____。
【答案】铁架台 分液漏斗 A 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 集气瓶口有气泡冒出,证明集满 二氧化锰 催化 过氧化氢
锰酸钾+二氧化锰+氧气 集气瓶口有气泡冒出,证明集满 二氧化锰 催化 过氧化氢![]() 水+氧气 可以控制反应的速率 不能 因为没有确认MnO2的质量和性质是否改变 MnO2质量的多少对H2O2分解的速率是否有影响
水+氧气 可以控制反应的速率 不能 因为没有确认MnO2的质量和性质是否改变 MnO2质量的多少对H2O2分解的速率是否有影响
【解析】
解:(1)通过分析题中所指仪器的名称和作用可知,①是铁架台,②是分液漏斗;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以应选用的发生装置是A,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气,氧气不易溶于水,密度比水小,所以选用E装置收集氧气时,判断集气瓶中已集满氧气的方法是:集气瓶口有气泡冒出,证明集满;
锰酸钾+二氧化锰+氧气,氧气不易溶于水,密度比水小,所以选用E装置收集氧气时,判断集气瓶中已集满氧气的方法是:集气瓶口有气泡冒出,证明集满;
(3)B装置制取氧气的反应物是固体和液体,反应条件是常温,锥形瓶内放入的固体物质通常是二氧化锰,是该反应的催化剂,起催化作用,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为:过氧化氢![]() 水+氧气,分液漏斗可以控制液体的滴加速度,所以B装置制取氧气的一个优点是:可以控制反应的速率;
水+氧气,分液漏斗可以控制液体的滴加速度,所以B装置制取氧气的一个优点是:可以控制反应的速率;
(4)要证明MnO2是H2O2分解反应的催化剂,必须证明催化剂在反应前后的性质和质量不改变,而甲同学没有做这方面的实验,所以不能达到目的;
(5)根据表格中数据,探究的目的是MnO2质量的多少对H2O2分解的速率是否有影响。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案