题目内容
12.金属材料在工农业生产、日常生活中有着广泛应用.①铁和铝都可以制作炊具,主要利用了它们的导热性.
②铝制品具有耐腐蚀性的原因是4Al+3O2═2Al2O3(用方程式表示)
③21世纪的能源金属-锂(Li)金属锂,被誉“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题:a.锂原子的原子结构示意图如图所示
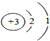 ;锂原子在化学反应中容易失去(填“得到”或“失去”)电子变成离子,其离子符号为Li+.
;锂原子在化学反应中容易失去(填“得到”或“失去”)电子变成离子,其离子符号为Li+.b.研究表明,锂的金属活动性比较活泼,能与稀硫酸反应.写出金属锂与稀硫酸反应的化学方程式2Li+H2SO4═Li2SO4+H2↑.
分析 ①根据铁和铝具有导热性进行分析;
②根据铝会与空气中的氧气反应来分析,书写其反应的化学方程式;
③a、最外层电子数多于4个易的电子,少于4个易失去电子;再根据离子的写法和化学式的写法考虑;
b、锂是一种活动性比铁强的金属,锂与稀硫酸反应生成硫酸锂和氢气,写出反应的化学方程式即可.
解答 解:①由于铁和铝具有导热性,所以都可以制作炊具;故答案为:导热;
②铝会与空气中的氧气反应生成了致密的氧化物薄膜,阻碍了氧化反应的继续进行具有很好的耐腐蚀性,故答案为:4Al+3O2=2Al2O3;
③a、最外层电子数是1,所以失去一个电子,带一个单位正电荷,写在锂元素的右上角数字在前,正负号在后,由于数字是1要省略不写;
b、锂是一种活动性比铁强的金属,锂与稀硫酸反应生成硫酸锂和氢气,反应的化学方程式为:2Li+H2SO4=Li2SO4+H2↑;
故答案为:a、失去;Li+;b、2Li+H2SO4═Li2SO4+H2↑.
点评 由题意,找出反应物和生成物、反应条件,根据质量守恒定律,正确书写化学方程式;了解化学性质与物理性质的差别及其应用.

练习册系列答案
相关题目
3.下列说法中,正确的是( )
| A. | 饱和溶液在温度升高时,一定能继续溶解溶质 | |
| B. | 相同温度下,饱和溶液一定比不饱和溶液浓 | |
| C. | 区分硬水和软水的方法:加等量的肥皂水,振荡,观察有无泡沫或泡沫多少进行区分 | |
| D. | 要确定室温时某溶液是否饱和的方法:室温时蒸发一部分水,观察有无晶体析出确定 |
17.下列有关实验现象描述不正确的是( )
| A. | 木炭在氧气中燃烧,发出白色火焰,生成二氧化碳 | |
| B. | 铁在氧气中燃烧,火星四射,生成黑色固体 | |
| C. | 红磷在氧气中燃烧产生大量白烟 | |
| D. | 加热铜绿时,绿色粉末逐渐变为黑色 |
1.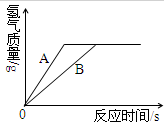 某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示.下列结论中合理的是( )
某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示.下列结论中合理的是( )
 某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示.下列结论中合理的是( )
某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示.下列结论中合理的是( )| A. | A表示铁和稀硫酸的反应曲线 | |
| B. | 反应结束后,A、B均反应完,硫酸有剩余 | |
| C. | 反应消耗Fe的质量小于Zn | |
| D. | 反应结束后所得溶液质量相等 |
2.在炼钢、医疗、宇航等生产、生活中都要用到的一种气体是( )
| A. | 氢气 | B. | 一氧化碳 | C. | 氧气 | D. | 氮气 |