题目内容
【题目】为了消除碘缺乏病,我国政府规定居民的食用盐必须是加碘食盐,简称碘盐.所谓碘盐就是在食盐中加入一定量碘酸钾(KIO3).图为“云鹤牌”精制碘盐包装袋上的部分说明文字,请回答下列问题:

(1)碘酸钾的相对分子质量为_____,碘酸钾中钾、碘、氧元素的质量比为_____,碘酸钾中碘元素的质量分数为_____.
(2)已知成人每天约需0.15mg碘,假设这些碘主要是从碘盐中摄取的.若1000g碘盐中含20mg碘,则成人每天需食用这种碘盐_____g.
(3)_____mg碘酸钾中含20mg的碘;
(4)用单质碘(I2)与氯酸钾(KClO3)发生反应可制得碘酸钾,同时生成氯气,该反应的化学方程式为_____,该反应属于_____反应(填化学基本反应类型).
【答案】(1)214; 39; 127; 48; 59.3%
(2)7.5g (3)33.7mg
(4)I2+2KClO3=Cl2+2KIO3;置换
【解析】
试题(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,碘酸钾相对分子质量=39+127+16×3=214;
利用各元素的质量比为各元素的相对原子质量与原子个数乘积之比,计算碘酸钾中钾元素、碘元素、氧元素的质量比=39:127:(16×3)=39:127:48;
根据物质中某元素的质量分数=![]() ×100%,可知
×100%,可知
碘酸钾中碘元素的质量分数=![]() ×100%=59.3%;
×100%=59.3%;
(2)1000 g碘盐中约含20 mg碘,设x克碘盐中约含0.15mg碘,则 x×![]() =0.15mg,解得 x=7.5g;
=0.15mg,解得 x=7.5g;
(3)含20mg碘元素的碘酸钾的质量=20mg÷![]() ×100%≈33.7mg;
×100%≈33.7mg;
(4)由反应物、生成物和反应条件可以写出化学方程式,碘和氯酸钾反应生成碘酸钾和氯气,故该反应的化学方程式为:I2+2KClO3=Cl2+2KIO3,该反应的反应物和生成物中各有一种单质和一种化合物,故属于置换反应。

【题目】兴趣小组利用提供的试剂:稀硫酸、澄清石灰水、氯化钠溶液、硫酸铜溶液和紫色石蕊溶液。探究酸 碱盐的性质。小清同学将氯化钠溶液加入到稀硫酸中没有观察到明显现象,而将混合溶液加热一段时间后, 意外地闻到刺激性气味。
(提出问题)刺激性气味的气体是什么?
(猜想与假设)猜想 1.可能是二氧化硫 猜想 2.可能是氯化氢 猜想 3.可能是氨气
大家讨论后认为猜想 3 不合理,依据是_____。
(查阅资料)SO2 和 CO2 的化学性质相似,都能使澄清灰水变浑浊。写出二氧化硫和氢氧化钙的反应的化 学方程式:_____。
(实验探究)如图所示,小诚将产生的气体通入紫色石蕊溶液中,观察到______,于是他认为猜想 2正确。
(评价与改进)小煜认为小诚的结论不科学,于是他利用提供的试剂通过实验确认了猜想 2 正确。
实验现象 | 实验结论 |
如图所示,将产生的气体_____ | _____ |
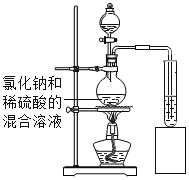
(结论)加热氯化钠与硫酸的混合溶液得到的气体是氯化氢
(拓展应用)实验室可用氯化钠和硫酸反应制取氯化氢气体,已知氯化氢气体极易溶于水。请推测实验室 制取氯化氢气体最适宜的方法为_____(填序号)。
A 加热氯化氢溶液和稀硫酸的混合物 B 加热氯化钠固体和稀硫酸的混合物 C 加热氯化钠固体和浓硫酸的混合物
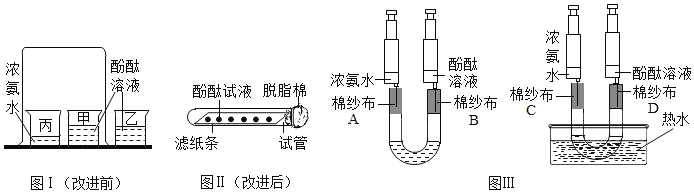
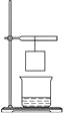
【题目】小华将一张滤纸在某示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图)放置一个盛有某溶液的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂和烧杯中的溶液分别是( )
A | B | C | D | |
滤纸上的指示剂 | 酚酞溶液 | 酚酞溶液 | 石蕊溶液 | 石蕊溶液 |
烧杯中的溶液 | 浓氨水 | 浓盐酸 | 浓氨水 | 浓盐酸 |
A. A
B. B
C. C
D. D
【题目】某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
(提出问题)澄清石灰水为什么没有变浑浊?
(查阅资料)
(1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2。
(2)AgCl不溶于稀硝酸。
(提出猜想)Ⅰ.石灰水已完全变质 Ⅱ.___________ Ⅲ.CO2中混有HCl
(实验方案)兴趣小组用原药品继续制取CO2,并进行探究。制备CO2的化学方程式为___________。
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 取少量澄清石灰水于试管中,加入______溶液。 | 生白色沉淀。 | 猜想Ⅰ不成立。 |
(2) | 将少量CO2气体通入盛有澄清石灰水的试管中。 | ___________。 | 猜想Ⅱ不成立。 |
(3) | 将气体通入盛有______溶液的试管中,再加稀硝酸。 | ___________。 | 猜想Ⅲ成立。 反应方程式为___________。 |
(实验结论)制取的气体CO2中混入了HCl,所以澄清石灰水没有变浑浊。
(交流讨论)若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和___________。
(拓展思考)回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是___________(写一点)。