题目内容
某研究性学习小组在学习金属铁的知识后,为了解铜及其常见化合物的性质,运用类比的思想提出了如下问题,并进行探究。请帮助完成下列有关研究并填写有关空白。
(1)【提出问题】
①铁能与稀硫酸反应产生氢气,铜能吗?铜与浓硫酸会发生反应吗?
②铁在潮湿的空气中易生锈,铜“生锈”需要什么条件?
③氧化铁能够被一氧化碳还原,氧化铜可以吗?氧化铜能直接转化为氢氧化铜吗?氧化铜还有哪些性质?
④有哪些途径可以由铜逐步转变为氢氧化铜?
(2)【查阅资料与问题解决】
①铜不能与稀硫酸发生置换反应,是因为在金属活动性顺序表中,铜排在 之后。
铜能与浓硫酸发生反应,其反应方程式为: Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑此反应中化合价升高的元素是 。
CuSO4+2H2O+SO2↑此反应中化合价升高的元素是 。
②铜在潮湿的空气中也能“生锈”形成铜绿,铜绿的主要成分为Cu2 (OH)2 CO3。由此可以推测:铜“生锈”过程中,参与反应的物质有铜、氧气、水和 。
③氧化铜可以在加热的条件下被一氧化碳等还原成铜,其与一氧化碳反应的化学方程式为 ;氧化铜不能与水反应生成氢氧化铜,但能与硫酸、盐酸等发生复分解反应形成相应的铜盐;在高温下,氧化铜能分解成砖红色的氧化亚铜(Cu2O)和氧气,反应的化学方程式为 。
④由铜转化为氢氧化铜,从化学反应的原理看,可以是流程I:

也可以是流程II:

与流程I相比,流程Ⅱ的优点是 和 。
还可以有更多的流程。若流程Ⅲ与流程I相比,也是两步反应,但第一步与铜反应的
试剂不同,则流程Ⅲ中第一步反应的化学方程式为 。
①氢.铜.
②二氧化碳.
③ CuO+CO Cu+CO2; 4CuO
Cu+CO2; 4CuO 2Cu2O+O2↑.
2Cu2O+O2↑.
④安全、环保.
Cu+2AgNO3=Cu(NO3)2+2Ag
【解析】
试题分析:(2)①在金属活动性顺序表中排在氢后面的金属不能与硫酸发生置换反应生成氢气。
在反应“Cu+2H2SO4(浓) △ CuSO4+2H2O+SO2↑”中铜元素的化合价由反应前的零价升高为反应后的+2价。
②铜绿的主要成分为Cu2 (OH)2 CO3,其中含有铜、氧、氢、碳等元素。所以铜“生锈”过程中,参与反应的物质除有铜、氧气、水之外,还应该有一种含碳元素且空气中含有的物质—二氧化碳。
③氧化铜可以在加热的条件下被一氧化碳等还原成铜,其与一氧化碳反应的化学方程式为:CuO+CO Cu+CO2;
Cu+CO2;
在高温下,氧化铜能分解成砖红色的氧化亚铜(Cu2O)和氧气,反应的化学方程式为:4CuO 2Cu2O+O2↑.
2Cu2O+O2↑.
④流程Ⅱ使用的是稀硫酸,与流程I使用浓硫酸相比的优点有:安全(浓硫酸的强腐蚀性)、环保(浓硫酸与铜反应生成的二氧化硫会造成空气污染)。
流程Ⅲ中第一步与铜反应的物质应为在金属活动性表中排在铜后面的金属的盐溶液,即硝酸银。所以反应的化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag
考点:科学探究
点评:本题结合科学探究考查了质量守恒定律、金属的化学性质、实验方案的设计等知识点。

复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验.
(1)探究1:研究常见物质组成

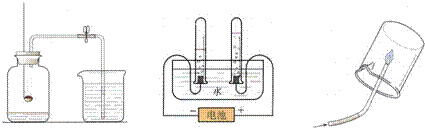
A.测定空气中的氧气含量 B.水电解实验 C.检验甲烷成分
A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的________,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的________来推断水的组成的.而C实验与________(填实验代号)实验的方法相同.
(2)探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
小明用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.他决定来验证一下:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,________ | ________ | 证明研究结论正确 |

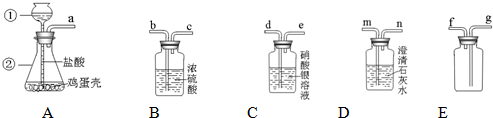
①根据我们所学的知识,你认为A装置和________装置相连并产生什么现象时就足以说明鸡蛋壳的主要成分是碳酸盐?________;写出该装置中发生反应的化学方程式:________.
②该同学想要收集一瓶纯净的该气体,进一步验证它的性质.连接上述装置的顺序是:(填写各接口字母)________.其中,C装置的作用是:________.
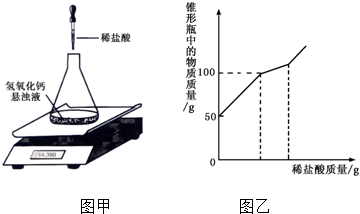
(4)某研究性学习小组在协助老师清理实验储备室时,发现一批存放多年的氢氧化钙.为检验其变质情况,进行了如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,振荡形成悬浊液,放在电子天平上,向锥形瓶中逐滴滴加14.6%的稀盐酸,振荡后读取质量(如图甲所示).实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图乙所示.

求:11.4g该样品中各成分的质量.
(1)探究1:研究常见物质组成

A.测定空气中的氧气含量 B.水电解实验 C.检验甲烷成分
A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的______,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的______来推断水的组成的.而C实验与______(填实验代号)实验的方法相同.
(2)探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
小明用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.他决定来验证一下:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,______ | ______ | 证明研究结论正确 |

①根据我们所学的知识,你认为A装置和______装置相连并产生什么现象时就足以说明鸡蛋壳的主要成分是碳酸盐?______;写出该装置中发生反应的化学方程式:______.
②该同学想要收集一瓶纯净的该气体,进一步验证它的性质.连接上述装置的顺序是:(填写各接口字母)______.其中,C装置的作用是:______.
(4)某研究性学习小组在协助老师清理实验储备室时,发现一批存放多年的氢氧化钙.为检验其变质情况,进行了如下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,振荡形成悬浊液,放在电子天平上,向锥形瓶中逐滴滴加14.6%的稀盐酸,振荡后读取质量(如图甲所示).实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图乙所示.

求:11.4g该样品中各成分的质量.