题目内容
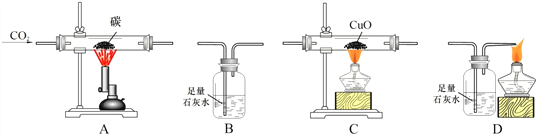
【题目】Ⅰ.如图是一氧化碳还原氧化铁实验装置图,回答下列问题:
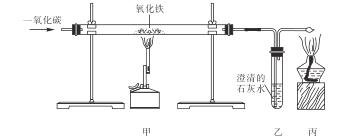
(1)写出甲处玻璃管中的反应化学方程式__________;
(2)下列关于该实验的说法正确的是__________ (填字母);
A.装置甲处玻璃管内黑色粉末变红
B.实验结束后,应先熄灭甲处的酒精喷灯,后熄灭丙处的酒精灯
C.一氧化碳发生了还原反应
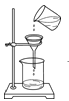
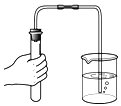
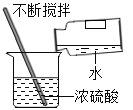
Ⅱ.图1是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:

(1)用图1的序号表示配制溶液的正确操作顺序为__________;
(2)操作③用玻璃棒搅拌的目的是__________;
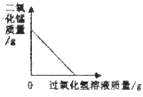
(3)称量NaCl时,天平平衡后的状态如图1中⑤所示,游码标尺示数见图2,需要NaCl固体__________g,需要量取水的体积是__________mL(水的密度为1g/mL);
(4)经检测,配制出来的NaCl溶液溶质质量分数偏小,其原因可能有__________ (填序号)。
①氯化钠固体不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
【答案】Fe2O3+3CO![]() 2Fe+3CO2 B ②⑤①④③ 加快溶解速率 18.2 163.8 ①②③
2Fe+3CO2 B ②⑤①④③ 加快溶解速率 18.2 163.8 ①②③
【解析】
Ⅰ.(1)一氧化碳能与氧化铁高温反应生成铁和二氧化碳,反应化学方程式:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(2)A、装置甲处玻璃管内红色粉末变黑,故错误;
B、实验结束后,应先熄灭甲处的酒精喷灯,故正确;
C、一氧化碳发生了氧化反应,故错误;
Ⅱ.(1)称量食盐的质量首先打开广口瓶塞,倒放在桌面上,将取得的食盐放在天平的左盘,然后将称得的食盐放到烧杯中,再将量取的水倒入烧杯中,用玻璃棒搅拌使之溶解,故正确的顺序为②⑤①④③;
(2)图③中,使用玻璃棒搅拌的作用是搅拌,加速溶解;
(3)食盐的质量=砝码+游码,据图可知,砝码的读数是15g,游码的读数是3.2g,故食盐的质量=15g+3.2g=18.2g;配溶液的质量为:![]() =182g,所以需要水的质量是182g-18.2g=163.8g,水的密度为1g/mL,即需要水的体积为163.8mL;
=182g,所以需要水的质量是182g-18.2g=163.8g,水的密度为1g/mL,即需要水的体积为163.8mL;
(4))①氯化钠固体仍然不纯,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小;
②称量时砝码端忘垫质量相同的纸片,氯化钠和纸片的质量等于砝码和游码的质量,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小;
③量取水时,仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小;
④溶液具有均一性,装瓶时,有少量溶液洒出,溶质质量分数不变。

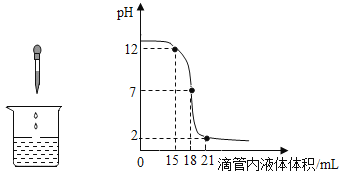
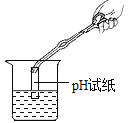
【题目】酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用,如图表示稀盐酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作,请从中获取信息,回答下列问题。
(1)①烧杯中盛放的是_____溶液。
②曲线上坐标为(15,12)的点所表示的意义:_____。
(2)小明完成上述实验几天后发现,忘记盖上盛放氢氧化钠溶液试剂瓶的瓶塞,请帮助小明完成如下实验方案来检验氢氧化钠溶液是否变质。
(提示:碳酸钠与氯化钡反应会生成碳酸钡沉淀和氯化钠)
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取少量溶液于试管中,滴加几滴稀盐酸 | _____ | 没有变质 |
方案二 | 取少量溶液于试管中,滴加几滴氯化钡溶液 | 产生白色沉淀 | 已经变质 |
你认为方案一的实验设计是否正确?请作出判断并说明理由:_____。