题目内容
【题目】某课外小组的同学用 10%的氢氧化钠溶液逐滴加入到50克稀盐酸中,边加边搅拌,随着氢氧化钠溶液的不断加入,溶液的 pH变化情况如图所示。
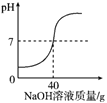
(1)计算pH= 7时,所得溶液的溶质质量分数__________。
(2)若将pH= 7时,所得溶液的溶质质量分数增大一倍,可采用的一种方法是__________,写出计算过程(最后结果精确到0.1)。
【答案】6.5%。方法一:蒸发溶剂
计算过程:设蒸发溶剂质量为y。
5.85 g=(90 g-y)×13% y=45.0 g
方法二:增加溶质
计算过程:设加入氯化钠质量为y。
![]() ×100%=13% y≈6.7 g
×100%=13% y≈6.7 g
【解析】
(1)pH=7表示酸碱刚好反应,生成物为NaCl,由图可知pH=7时,NaOH的质量为40g,计算可知钠元素的质量为40×10%×![]() =2.3g,pH=7时,氯化钠的质量为2.3×
=2.3g,pH=7时,氯化钠的质量为2.3×![]() =5.85g则总质量为90g百分含量为
=5.85g则总质量为90g百分含量为![]() ×100%=6.5%,
×100%=6.5%,
(2)增大溶液质量分数为2倍,可以通过增加溶剂和减少溶剂的方法,计算如答案所示。

 名校课堂系列答案
名校课堂系列答案【题目】空气质量预报主要内容包括:首要污染物、空气污染指数和空气质量级别.空气污染与空气质量级别的对应关系(表![]() )
)
空气污染指数 |
|
|
|
|
|
|
|
空气质量状况 | 优 | 良 | 轻度污染 | 轻度污染 | 轻度污染 | 重度污染 | 重度污染 |
空气质量级别 |
|
|
|
|
|
|
|
![]() 年
年![]() 月
月![]() 日我国部分城市空气质量日报(表
日我国部分城市空气质量日报(表![]() )
)
城市 | 首要污染物 | 空气质量指数 | 空气质量级别 |
广州 | 可吸入颗粒物 |
|
|
天津 | 可吸入颗粒物 |
| ① |
昆明 | 二氧化硫 |
|
|
海口 | – |
|
|
![]() 上述城市中易出现酸雨的城市是________;
上述城市中易出现酸雨的城市是________;
![]() 请根据表
请根据表![]() 和表
和表![]() 的内容,确定当日天津的空气质量级别:①________.
的内容,确定当日天津的空气质量级别:①________.
![]() 为了提高广州的空气质量,请你至少提出两项可以提高广州空气质量的措施:
为了提高广州的空气质量,请你至少提出两项可以提高广州空气质量的措施:
①________;②________.
【题目】下面呈现的是某实验小组在课堂上做的一组探究实验:
(1)在a试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的现象是_____。
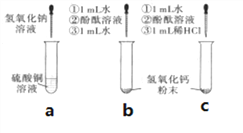
(2)向b、c两支试管中各加入少量相同质量的氢氧化钙粉末,然后各加入1mL水,振荡,呈浑浊状,静置,再各滴入1~2 滴酚酞溶液,观察到两试管溶液均变红。继续向b试管中加入约1mL水振荡;向c试管中加入约1mL稀盐酸,振荡。发现b试管变澄清,溶液仍呈红色,c试管变澄清,溶液变成无色。向b试管中第二次加入约1mL水的作用是________。
(提出问题)试管c中加入约1mL稀盐酸后,溶液中的溶质是什么?
(查阅资料)查阅资料:CaCl2溶液呈中性。
(猜想假设)小丽猜想:I.CaCl2 Ⅱ.CaCl2和HCl Ⅲ.CaCl2和Ca(OH)2
(反思质疑)小明对猜想Ⅲ产生质疑,理由是___________
(进行实验)小组同学通过交流,设计如下实验方案进行验证:
实验步骤 | 实验现象 | 实验结论 |
取少量c试管中的溶液于试管中,_______ | ________ | 猜想Ⅱ成立 |
实验结束,小组同学将a、b、c三支试管中的剩余物质混合,发现废液呈浑浊。
(问题与交流)废液中大量存在的阳离子有_______。写出废液中可能发生反应的一个化学方程式________。
【题目】学习了溶液的概念后,老师的提问及同学的回答如下图所示:

![]() 以上三位同学中能够正确描述溶液特征的是________同学.老师接着问:“你们还想知道什么?”王华回答:“影响物质在水中溶解能力的因素有哪些?”
以上三位同学中能够正确描述溶液特征的是________同学.老师接着问:“你们还想知道什么?”王华回答:“影响物质在水中溶解能力的因素有哪些?”
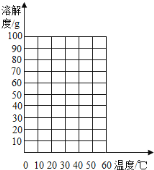
![]() 针对王华的问题,老师引导同学们进行了一系列探究,下表列出了从探究实验中获取的部分数据,请你根据这些下表中的数据,在右边的坐标图中绘制
针对王华的问题,老师引导同学们进行了一系列探究,下表列出了从探究实验中获取的部分数据,请你根据这些下表中的数据,在右边的坐标图中绘制![]() 、
、![]() 两物质的溶解度曲线(图中注明
两物质的溶解度曲线(图中注明![]() 、
、![]() ).________
).________
温度 |
|
|
|
| |
溶解度 |
|
|
|
|
|
|
|
|
|
| |
![]() 该实验主要探究了温度对固体物质溶解度的影响,在一定温度范围内,
该实验主要探究了温度对固体物质溶解度的影响,在一定温度范围内,![]() 物质的饱和溶液溶质质量分数大于
物质的饱和溶液溶质质量分数大于![]() 物质的饱和溶液溶质质量分数,该温度范围是________.
物质的饱和溶液溶质质量分数,该温度范围是________.
![]() 将在
将在![]() ゜
゜![]() 时等量的
时等量的![]() 、
、![]() 饱和溶液同时降温到
饱和溶液同时降温到![]() ゜
゜![]() ,则析出晶体的质量
,则析出晶体的质量![]() ________
________![]() (填“大于”、“等于”或“小于”).
(填“大于”、“等于”或“小于”).
![]() 在
在![]() ゜
゜![]() 时,向
时,向![]() 水中加入
水中加入![]() 物质充分溶解后,形成的
物质充分溶解后,形成的![]() 物质溶液质量是________
物质溶液质量是________![]() .
.