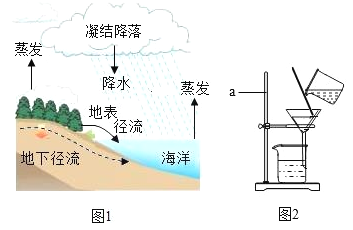
题目内容
过氧化钙(CaO2)是一种重要的化工产品,能杀菌消毒,广泛用于果蔬保鲜、 空气净化、污水处理等方面。某兴趣小组同学对其进行了有关探宄。
(查阅资料)
(1)过氧化钙是白色、无毒、难溶于水的白色粉末。
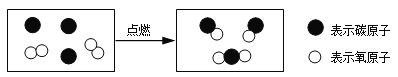
(2)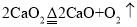 。
。
(3) ;二氧化锰与稀盐酸不反应。
;二氧化锰与稀盐酸不反应。
(探宄1)验证过氧化钙受热分解的产物。
(1)取少量纯净的过氧化钙放入试管中充分加热,将带火星的木条伸入试管,可观察到带火星的木条_______。
(2)待(1)中试管冷却,取管中少量固体加水充分搅拌,静置,向上层清液中滴加几滴酚酞试液,可观察到溶液变成_________色。
(探宄2)测定产品中过氧化钙的质量分数(假设过氧化钙产品中只含有氧化钙杂质)。
(实验装置)
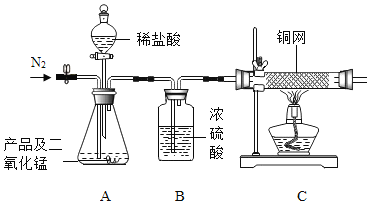
(实验步骤)
①连好装置并检查装置的气密性,在锥形瓶中放入4g该产品;②实验前称量C中铜网的质量;③先缓慢通入氮气,一段时间后加热铜网至红热;再缓慢滴入过量稀盐酸,直至A中样品完全反应;④继续缓慢通入氮气,一段时间后停止加热,待C中铜网冷却后,停止 通入氮气;⑤再次称量C中铜网的质量,发现比反应前増重0.8g。
(实验结论)
(1)A中二氧化锰的作用是____________________。
(2)C中铜网发生反应的化学方程式为______________。
(3)该产品中过氧化钙的质量分数为___________。
(拓展提升)若A中样品完全反应后,立即停止通氮气并熄灭酒精灯,待C中铜网冷却后称量其质量。你认为该操作对测定产品中过氧化钙的质量分数是否有影响?_____________。(选填“是”或“否”,并说明理由)。
练习册系列答案
相关题目