题目内容
【题目】下列有关说法正确的是( )
A. CO2的摩尔质量是44
B. 质量相同的SO2、SO3分子中硫原子个数比为4:5
C. 一个水分子的质量约为18÷(6.02×1023)g
D. 1mol N2约含6.02×1023个氮原子
【答案】C
【解析】
A、二氧化碳的摩尔质量为44g/mol,数值上等于相对分子质量,单位为g/mol,故A错误;
B、质量相等的SO2、SO3分子中硫原子个数比=![]() ,而非4:5,故B错误;
,而非4:5,故B错误;
C、1mol的水分子的个数为6.02×1023, 1mol的水分子的质量为18g,所以一个水分子的质量约为18÷(6.02×1023)g,故C正确;
D、1mol N2约含6.02×1023个氮分子,不是氮原子,故D错误。故选C。

【题目】把4 g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示。
| 第一次 | 第二次 | 第三次 |
氧气的质量(g) | 3 | 4 | 6 |
SO2的质量(g) | 6 |
|
|
请回答下列问题:
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是________;
(2)请你通过计算,求出第二次实验生成二氧化硫的质量_______;
(3)在表中填写第三次生成的二氧化硫的质量_______。
【题目】材料一:候德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:

①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成 NaHCO3晶体和NH4Cl溶液。
②将①中的产物 NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
NaCl | NH4Cl | NaHCO3 |
36.0 | 37.2 | 9.6 |
请回答下列问题:
(1)在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是_____。
(2)该生产过程中部分生成物可作为原料循环使用的是_____,同时得到的副产品NH4Cl是一种氮肥。
【题目】研究性学习小组选择下列某些仪器制取气体。
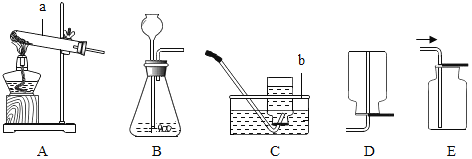
(1)写出仪器名称a_____、b_______
(2)该小组同学用加热高锰酸钾制取氧气。化学反应方程式为_____,此时发生装置应该选用上图中的_____,收集氧气的装置可以用_____。
(3)A装置中试管口略向下倾斜的原因是_____。
(4)若用B装置制取二氧化碳,使用了长颈漏斗的好处是______
(5)实验室常用硫化亚铁固体与稀硫酸在常温下反应制硫化氢气体和硫酸亚铁。由此可推知:实验室制取硫化氢气体时,发生装置应选用如图所示的(填代号)_____装置。
实验序号 | 大理石 (各6g) | 稀盐酸的浓度 | 反应开始到5分钟产生CO2的质量 | 反应结束产生的CO2的质量 |
① | 块状 | 16% | 2.16g | 2.2g |
② | 块状 | 9% | 1.42g | 2.2g |
③ | 粉末 | 16% | 2.33g | 2.2g |
④ | 粉末 | 9% | 1.93g | m 2 |