题目内容
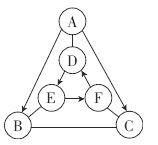
【题目】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示-——表示物质两两之间能发生化学反应。请根据如图,回答问题。(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)
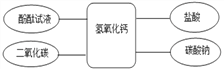
(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈_________________(填“酸性、碱性或中性”)。
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是________________,此时含有的溶质有________(酸碱指示剂除外)(用化学式填空,下同)。
(3)为验证乙同学所得溶液中含有的溶质,可取少量反应后的溶液滴加过量的____________溶液(填一种物质的化学式),产生_______________________________现象,则证明存在。
【答案】 碱性 溶液由红色变为无色 CaCl2和HCl Na2CO3 溶液由无色变为红色、溶液中有气泡生成、底部有白色沉淀生成
【解析】(1)酚酞试液遇碱性溶液变红。(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,稀盐酸剩余,溶液显酸性,酚酞遇酸性溶液不变色,故实验现象是溶液由红色变为无色。2HCl+ Ca(OH)2 ==CaCl2 +2H2O, 溶液中含有的溶质有生成的CaCl2 、剩余的HCl。(3)Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑,Na2CO3 + Ca(OH)2 == CaCO3 ↓+ 2NaOH,NaOH溶液显碱性,酚酞遇碱性溶液变红,故实验现象是溶液中有气泡生成、底部有白色沉淀生成、溶液由无色变为红色。

【题目】珍珠除了用于制作首饰外,还可制成珍珠粉入药。珍珠的主要成分是碳酸钙。某兴趣小组同学称取11.00g珍珠样品,将120.00g稀盐酸平均分成六次加入(假设珍珠中其它成分不与盐酸反应),测定每次加入稀盐酸充分反应后,产生二氧化碳的总质量如下表所示:
加入稀盐酸的次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加入稀盐酸的质量/g | 20.00 | 20.00 | 20.00 | 20.00 | 20.00 | 20.00 |
充分反应生成二氧化碳的总质量/g | 0.88 | 1.76 | 2.64 | 3.52 | 4.40 | 4.40 |
(1)第6次加入稀盐酸后,产生二氧化碳的质量不继续增加的原因为___________。
(2)计算该珍珠样品中碳酸钙的含量(即珍珠中碳酸钙的质量占珍珠质量的百分数为______,精确到0.1%)