题目内容
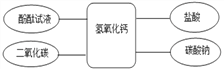
【题目】A~F是初中化学常见的物质,物质之间的部分反应及转化关系如下图所示,图中“→”表示转化关系,“-”表示相互反应。已知A、D、F是酸碱盐中的一种,其余的为氧化物,A是胃液的主要成分,E为建筑材料。
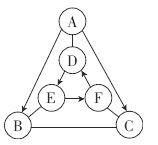
(1)A的化学式为___,F的俗称为____。
(2)E的用途为______。
(3)B和C___(填“一定” “不一定”“一定不”)是化合反应。
(4)A生成B可能的化学反应方程式为_________。
【答案】 HCl 熟石灰 食品干燥剂 不一定 CaCO3+2HCl==CaCl2+H2O+CO2↑
【解析】(1)A是胃液的主要成分,E为建筑材料,故A为HCl;E为建筑材料且是氧化物,故E是氧化钙(CaO),可以做干燥剂;
(2)E能生成F,故F为Ca(OH)2,俗称为熟石灰;F能生成D,D能与HCl反应,故D是CaCO3;
(3)A能生成B,B能和E反应,故B可能是水或氢气, A能生成C,C能与F反应,故C为二氧化碳,故B和C 的反应不一定是化合反应;
(4)当B是水时,反应方程式为CaCO3+2HCl==CaCl2+H2O+CO2↑;

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案【题目】铁、铝、铜是常见的三种金属.同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
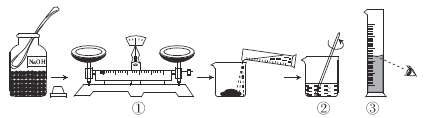
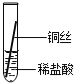
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
操作 |
|
|
| 根据现象得出金属活动性顺序 |
片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 | |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面的氧化物会先与盐酸反应.
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是 .
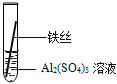
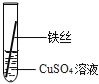
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出金属活动性顺序 |
现象 | 无明显现象 | | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式 .
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为 .
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序 .