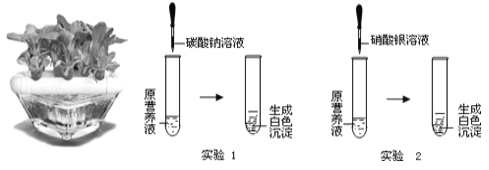
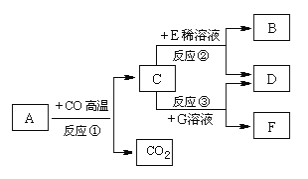
��Ŀ����
����Ŀ��(5��)ij��ѧ��ȤС���ѧ�������ֽ���R���ڳ���ѧ���Ľ������˳����У���С��Ϊ���˽�R�볣����������ͭ�Ľ������˳��������̽�����
���������롿���ǿ��ǵ����Ļ�Ա�ͭǿ�������ֽ����Ļ��˳���������²��룺
����һ��Al>Cu>R��������� ����������R> Al>Cu��
���������ϡ�R��һ������ɫ�Ľ�������R������Һ��ֻ��+2��R������Һ����ɫ�����������ı�����γ�һ�����ܵ�����Ĥ�����������Ȼ���������������Һ��Ϊ��ɫ��
��ʵ��̽����Ϊ��̽����һ�ֲ���������ס��ҡ�����λͬѧ�ֱ���Բ���һ������������������ʵ�鷽����չ��ʵ��̽����
���� | ��Ҫ���� | ��Ҫ���� | ʵ����� |
����һ | ��ĥR˿����������뵽����ͭ��Һ��. | R˿���渲����һ���ɫ������. | ����һ (���������������) |
����� | ��ĥ��ϸ��ͬ��R˿����˿��ͭ˿���ֱ����Dz��뵽�����ͬ��������������Ҳ��ͬ��ϡ������. | ��R˿����������ݻ�������Һ����ɫ�����ɫ. ����˿����������ݽϿ�. ��ͭ˿����û�����ݲ���. | ���������. |
������ | ����ĥ������˿���뵽 ��Һ��. | ����������. | ���������� |
 ��������˼���������ֲ����������λͬѧ�����۽��������ֱ�ͬѧ��ʵ��ǰû�д�ĥ��˿������ܻᵼ��ʵ����۴������������ȴ�ĥ��˿���ٽ�����뵽��ͬѧ��ʵ���ù�����Һ�У�һ��ʱ�����Һ����ɫ ������ȷ�ϲ�������������������������
��������˼���������ֲ����������λͬѧ�����۽��������ֱ�ͬѧ��ʵ��ǰû�д�ĥ��˿������ܻᵼ��ʵ����۴������������ȴ�ĥ��˿���ٽ�����뵽��ͬѧ��ʵ���ù�����Һ�У�һ��ʱ�����Һ����ɫ ������ȷ�ϲ�������������������������
�������ܽ̽�������������ܽ�ó���ͨ�������� ��Ӧ�����������Һ��Ӧ���ԱȽϽ������ǿ����
���𰸡����������롿Al>R>Cu (��Cu<R<Al)
��ʵ��̽������������ RSO4[��RCl2��R(NO3)2]��
��������˼����dz����ɫ����ȥ��
�������ܽ��.
��������
���������
���������롿������֪���Ļ�Ա�ͭǿ���ʽ���R�Ļ�Կ��ܴ����������������Al>Cu>R��Al>R>Cu��R> Al>Cu��
��ʵ��̽������ĥR˿����������뵽����ͭ��Һ�У�R˿���渲����һ���ɫ�����ʣ�˵��R�ܽ�ͭ�û���������R�Ļ�Ա�ͭǿ������һ����Ҫ֤��R�Ļ�Ա���ǿ��ֻ��Ҫ����˿����R����Һ�У���R�ı���û�з����κα仯��˵�����Ļ�Ա�R������������ȷ��
��������˼��������������Ӧ�������ܵ���������Ĥ����Ҫͨ����ĥ�ѱ������������ȥ���ٰ�������R����Һ�У�����Һ����ɫ�����˱仯��˵�����Ļ�Ա�Rǿ������������
�������ܽ�����Ļ��Խǿ�����ᷴӦԽ���ң��ʿ�ͨ���������ᷴӦ�۲��������ᷴӦ�ľ��ҳ̶����жϽ����Ļ�ԡ�

����Ŀ��ij��ѧС���ڿ���ʱ����һ��ʵ�飬�ڼ��Թ���װ��������ʣ����Թ���װ��Һ���Լ�������ͼ��ʾ��װ��������ͼ������̨����������ȥ����ͨ����Һ©����������ϡ���ᣬͬʱ��ֹˮ�У��������Թ�Һ����������ð����һ��ʱ���ر�ֹˮ�У���������ҳ����������Һ����ǡ���������ʵ�������һ���Լ���
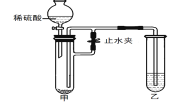
ѡ�� | ���еĹ��� | �����Լ� |
A | Cu | KOH |
B | Zn | Ba��NO3��2 |
C | Na2CO3 | NaOH |
D | KNO3 | BaCl2 |