题目内容
【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法正确的是( )

A. t1℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等,且都等于 60%
B. t2℃时,甲、乙两种物质的饱和溶液,降温至t1℃,析出晶体质量,甲不一定大于乙
C. t1℃时,将甲、乙两种物质的饱和溶液升温至t2℃时,溶质的质量分数甲大于乙
D. t1℃时,将甲、乙两种物质的饱和溶液分别降温到0℃,乙析出晶 体比甲析出晶体多
【答案】B
【解析】
A、由溶解度曲线可知,t1℃时,甲、乙两物质的溶解度相等为60g。故t1℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等,且都等于![]() ×100%= 37.5%,选项错误;
×100%= 37.5%,选项错误;
B、由于甲、乙两种物质的饱和溶液的质量不确定,故t2℃时,甲、乙两种物质的饱和溶液,降温至t1℃,析出晶体质量,甲不一定大于乙,选项正确;
C、由溶解度曲线可知,t1℃时,甲、乙两物质的溶解度相等,溶质质量分数相等,溶解度随温度的升高而增大。由t1℃升温至t2℃时,温度升高,甲、乙两种溶液中溶质、溶剂质量不变,故溶质质量分数不变,选项错误;
D、由于甲、乙两种物质的饱和溶液的质量不确定,故t1℃时,将甲、乙两种物质的饱和溶液分别降温到0℃,甲、乙析出晶体的质量无法比较,选项错误。故选B。

 考前必练系列答案
考前必练系列答案【题目】途运输鱼苗时,常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙的时产生气泡。
(査阅资料)氢氧化钙的水溶液就是石灰水。
(提出问题)当把过氧化钙投入足量水中时,最终生成什么物质?
(进行猜想)甲同学:生成碳酸和氧气;
乙同学:生成氢氧化钙和氧气。
同学和老师都认为甲同学的猜想是错误的,其理由是________。
(实验探究)
(1)打开下图装置中分液漏斗的活塞,控制滴加水速度,观察到试管内有气泡产生。
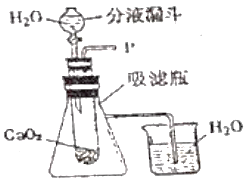
①___________(填实验操作),说明生成的气体是氧气。
②实验过程中,发现烧杯中有气泡出现,该现象说明___________。
(2)请设计一个实验方案来验证过氧化钙和水反应产生的另一种物质是氢氧化钙:
实验步骤及操作方法 | 预期的实验现象 | 结论 |
①取少量过氧化钙放入试管中,加足量水,震荡,②往所得溶液中通入____________。 | ①产生气泡, ②_________。 | 过氧化钙和水反应产生的另一种物质是氢氧化钙 |
(问题讨论)
(1)运输鱼苗时,在水中加入少量过氧化钙的主要目的是________;
(2)过氧化钙和水反应的化学方程式为____________。