题目内容
【题目】Ca(HCO3)2![]() CaCO3 +CO2 +H2O,是石灰岩溶洞形成的主要反应。将 1molCa(HCO3)2 加热 t2 秒时停止加热。如图表示 0→t2 秒过程中固体的物质的量随时间变化情况(该过程的 CaCO3 不分解)。说法错误的是( )
CaCO3 +CO2 +H2O,是石灰岩溶洞形成的主要反应。将 1molCa(HCO3)2 加热 t2 秒时停止加热。如图表示 0→t2 秒过程中固体的物质的量随时间变化情况(该过程的 CaCO3 不分解)。说法错误的是( )
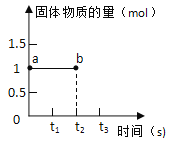
A.0→t2 反应阶段,固体 a、b 的物质的量不变
B.0→t2 反应阶段,固体a、b 的质量变小
C.a、b 两点固体中钙元素物质的量一定相等
D.固体a、b 中所含碳元素物质的量的比值一定为 2:1
【答案】D
【解析】
A、1molCa(HCO3)2 加热生成1mol CaCO3,故0→t2 反应阶段,固体 a、b 的物质的量不变,正确;
B、随着反应进行,Ca(HCO3)2 分解成了二氧化碳气体和水,故0→t2 反应阶段,固体a、b 的质量变小,正确;
C、反应过程中钙元素并未发生逸出等情况而造成物质的量减少,故a、b 两点固体中钙元素物质的量一定相等,正确;
D、无法判断b点的固体是否已经反应完全,故固体a、b 中所含碳元素物质的量的比值不一定为 2:1,错误。
故选D。

【题目】请通过下列四组实验,回答相关问题:
甲 | 乙 | 丙 | 丁 |
|
|
|
|
铁丝燃烧 | 测定水的元素组成 | 煅烧石灰石 | 测定空气中氧气体积分数 |
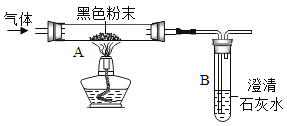
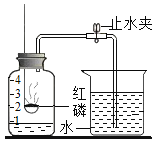
(1)实验甲中,铁丝在氧气中燃烧的现象是_____,反应的化学方程式_____;该实验瓶底 留少量水的目的是_____。
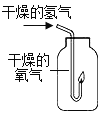
(2)实验乙中,观察到集气瓶内壁有_____产生,也可以得出结论。氢气燃烧的化学方程式_____。
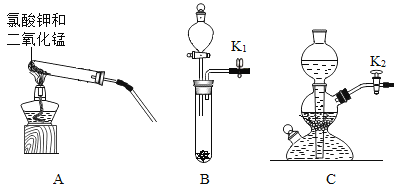
(3)实验丙中,观察到烧杯内壁石灰水变浑浊,写出产生此现象的反应的化学方程式_____。实验结论:说明石灰石已分解。该实验设计是否合理,理由是_____。
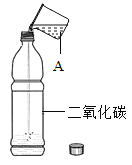
(4)实验丁中,红磷燃烧的化学方程式是_____,冷却到室温,打开止水夹,观察到的现象是_____。若测定氧气的体积分数偏小,可能的原因是_____。
【题目】学习金属化学性质时,小红同学对“锌与硫酸反应快慢的影响因素”进行了探究。锌与硫酸反应的化学方程式是_____。
(提出问题)锌与硫酸反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
(设计并实验)小红用不同质量分数的硫酸和不同形状的锌进行下表所示实验。
实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积/mL(均集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(收集证据)
(1)比较不同形状的锌对反应快慢的影响,选拌的实验编号是_____。
(2)比较不同质量分数的硫酸对反应快慢的影响,选择的实验编号是_____。
(得出结论)结论是①_____;②_____。
(评价与反思)
(l)下表是小组同学第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第6分钟 |
H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 6.0mL |
第2分钟以后反应变慢是因为______________。
(2)实验结束发现实验用的试管内有白色晶体,显然不是剩余的锌,它应该是_____,产生这些白色晶体的原因是_____。