题目内容
【题目】如图所示,将滴有酚酞溶液的滤纸放在试管中,试管口塞上一团脱脂棉.(提示:酚酞遇氨水变红色)

(1)用仪器A吸取浓氨水,滴在脱脂棉上(10~15滴)A的名称是____,其用途是______.
(2)实验中,观察到的现象是________,这说明了_________.
(3)某同学做此实验时,发现滤纸条上没有变色,而试管中所塞的脱脂棉却变成了红色.导致这种现象产生的错误操作可能是______,这一实验还说明,两种试剂中______具有挥发性.
【答案】胶头滴管 吸取或滴加少量液体 滤纸条从右到左逐渐变红 氨分子是不断运动的 药品放反了 浓氨水
【解析】
(1)由图可知,仪器A用来吸取或滴加少量液体,化学上常用胶头滴管来吸取或滴加液体,故填胶头滴管;
化学上常用胶头滴管来吸取或滴加液体,故填吸取或滴加液体。
(2)实验中观察到的现象是滤纸条从右到左逐渐变红,故填滤纸条从右到左逐渐变红;
氨气分子不断地运动,氨分子从试管右端向左端运动,依次与酚酞溶液中的水接触形成氨水,氨水显碱性,使滤纸条上的酚酞溶液由右向左依次变红,故填氨分子是不断运动的。
(3)滤纸条上没有变色,而试管中所塞的脱脂棉却变成了红色,说明滤纸上滴加了浓氨水,而脱脂棉上滴加了酚酞溶液,即两种药品放反了,故填药品放反了;
实验中,变红的是酚酞溶液,而滴加浓氨水的脱脂棉或滤纸条不变红,说明具有挥发性的位置是浓氨水,故填浓氨水。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
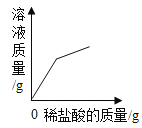
名题训练系列答案【题目】为探究盐酸的化学性质,某化学小组做了如下实验:

(1)A试管中的实验现象为_____,C试管中所发生反应的化学方程式为_____。
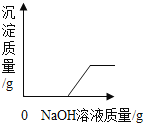
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
(提出问题)滤液中溶质的成分是什么?
(作出猜想)猜想一:NaCl 猜想二:NaCl和CaCl2
猜想三:_____ 猜想四:NaCl、Ca(OH)2和HCl
(交流讨论)同学们经过讨论后一致认为猜想_____不正确。
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液。 | _____ | 猜想二不成立 |
取少量滤液于试管中,滴加_____(填名称)。 | _____ | 猜想三成立 |
【题目】市场上有一种名为“污渍爆炸盐”的洗涤产品,它能高效去除衣物上的顽固污渍。小明对这种产品产生了兴趣,与小刚进行了如下探究。
(查阅资料)(1)“污渍爆炸盐”的主要成分是过碳酸钠(2Na2CO3 ·3H2O2),易溶于水且能与水反应生成一种碱性物质和一种强氧化性的物质;
(2)过碳酸钠的去污能力主要与其在反应中释放出的“活性氧”有关,“活性氧”含量越高,去污能力越强。
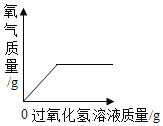
(实验1)小明向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,该气体能使带火星的
木条复燃,反应的化学方程式是___________。
(提出问题)实验1反应后的溶液中溶质的成分是什么?
(做出猜想)根据过碳酸钠和水的组成作出三种猜想。
猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH
(实验2)为证明猜想一是否正确,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
小明取一定量溶液于试管中,向其中滴加CaCl2溶液 | 有白色沉淀 | 猜想一正确 |
小刚提出质疑,认为产生的白色沉淀不一定是CaCO3。他的理由是______。
(实验3)为证明猜想二是否正确,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
小刚取一定量溶液于试管中,向其中滴加足量稀盐酸 | 观察到___ | 溶液中一定含有Na2CO3,猜想二不正确 |
Na2CO3与稀盐酸反应的化学方程式是_____________。
(实验4)为进一步确定溶液中是否含有NaOH,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
向实验1反应后的溶液中滴加CaCl2溶液至不再产生沉淀为止,取上层清液,加入____ | 无明显现象 | 证明溶液中无NaOH,猜想一正确。 |
该实验中用CaCl2溶液而不能用石灰水,原因是___________。
【题目】同学们在实验室用下图装置制取氧气。
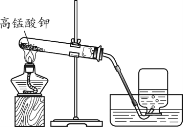
(1)加热高锰酸钾时,试管口略向下倾斜的原因是______。
实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
(查阅资料)
草酸溶液能将棕褐色物质除去。
(提出问题)
哪些因素能加快草酸除去棕褐色物质的速率?
(进行实验)
将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
实验 编号 | 实验1
20℃ 水 | 实验2
20℃ 0.5%草酸溶液 | 实验3
20℃ 0.25%草酸溶液 | 实验4
20℃ 0.125%草酸溶液 | 实验5
30℃ 0.25%草酸溶液 | 实验6
40℃ 0.25%草酸溶液 |
现象 | 颜色 没有褪去 | 70秒后 颜色褪去 | 98秒后 颜色褪去 | 150秒后 颜色褪去 | 51秒后 颜色褪去 | 40秒后 颜色褪去 |
(解释与结论)
(2)配制200g溶质质量分数为 0.5%的草酸溶液,需要草酸的质量为______。
(3)实验1的目的是______。
(4)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比______(填实验序号)。
(5)由实验2、3、4可以得出的结论是______。
(反思与评价)
(6)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证______。