题目内容
用某金属颗粒与足量的稀硫酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是
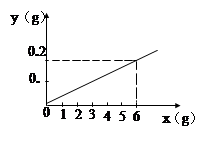
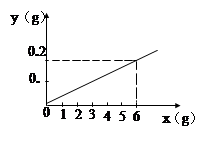
| A.纯净的锌 |
| B.含铜的锌 |
| C.含有不与酸反应杂质的铁 |
| D.含有不与酸反应杂质的锌 |
C
试题分析:从图中可以看出:当金属质量为6g时,产生的氢气质量为0.2g,再根据金属与酸反应的通式:假设金属符号为R,则化学方程式为:R+2HCl=RCl2+H2↑,根据方程式中金属与氢气的质量关系可列式为:R:2=6g:0.2g,则金属的平均相对原子质量R=60,则不是纯净的锌,应是混合物,且一种金属的相对原子质量应大于60,另一种金属的相对原子质量应小于60,故选C

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 H2
H2  Cu; (2)CuO
Cu; (2)CuO Cu
Cu

