题目内容
【题目】下表是生活饮用水国家标准的部分内容。
生活饮用水水质常规检验项目及限值(部分)
项目 | 限值 |
色度 | 不超过15度,并不得呈现其他异色 |
浑浊度 | 不超过1度,特殊情况下不超过5度 |
pH | 6.5~8.5 |
总硬度(以CaCO3计) | 450mg/L |
铝 | 0.2mg/L |
铁 | 0.3mg/L |
硫酸盐 | 250mg/L |
①表中“铝”指的是_______(选填“单质”“元素”或“原子”)。
②生活中硬水软化的方法是________ ,若想知道该水是硬水还是软水,可加入________ 来检验。
③Cl2、ClO2均可作自来水消毒剂,其中氯元素的化合价分别是____________。
④1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量不超过____mg/L。
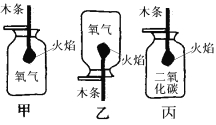
⑤实验室用上述水样通电分解,产生氢气和氧气的体积比约为_______;反应的化学方程式为 :________。
⑥地球上的总水储量虽然很大,但淡水很少,爱护水资源是每个公民应尽的责任和义务。请你列举一条节约用水的合理建议:_________。
【答案】元素 煮沸 肥皂水 0、 +4 180 2:1 2H2O![]() 2H2 ↑+ O2↑ 淘米水浇花(合理即可得分)
2H2 ↑+ O2↑ 淘米水浇花(合理即可得分)
【解析】
①食品、药品、营养品、矿泉水等物质中的“铁、铝”等不是以单质、分子、原子、离子等形式存在,这里所指的“铝”是强调存在的元素,与具体形态无关;
②加热煮沸能减少水中钙、镁离子的化合物的含量。所以,生活中常用的硬水软化的方法是煮沸;若想知道该水是硬水还是软水,可加入肥皂水来检验。泡沫少、起浮渣的是硬水,泡沫多、无浮渣的是软水;
③Cl2是单质,其化合价为0;ClO2中氧元素显-2价,则氯元素的化合价为[0-(-2×2)]=+4;
④由题目信息可知,1L合格的生活饮用水中,CaCO3的质量不能超过450mg,则钙元素的含量应不超过:450mg×![]() =180mg/L;
=180mg/L;
⑤电解水实验中产生氢气和氧气的体积比约:2:1;水在通电的条件下生成氢气和氧气,反应的化学方程式为:2H2O![]() 2H2 ↑+ O2↑;
2H2 ↑+ O2↑;
⑥淘米水浇花、用完水后及时关闭水龙头等都是节约用水的表现。

 教材全解字词句篇系列答案
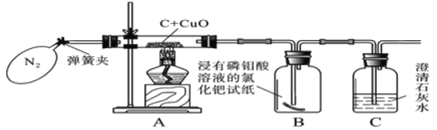
教材全解字词句篇系列答案【题目】空气是一种宝贵资源,如利用空气中分离出的氮气合成氨气,合成氨对社会发展和人类进步做出了巨大贡献,下列是合成氨的工艺流程图:
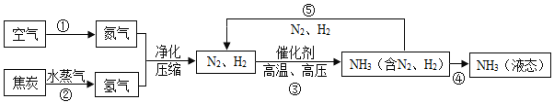
(1)空气属于____(填“纯净物”或“混合物”),空气中氮气的体积分数约为 __%。
(2)用化学用语填空
两个氢分子____ 标出NH3中氮元素的化合价______
氦气__________ 步骤③的反应中没有改变的微粒是__
(3)将沸点不同的气体分离开来,常采用液化分离法。如控制温度在﹣183℃时,可将空气中N2与O2分离。根据下表中物质的沸点判断,要将产物NH3与N2、H2分离开来,温度应该控制在___℃。
物质 | H2 | N2 | O2 | NH3 |
沸点 | ﹣252℃ | ﹣195.8℃ | ﹣183℃ | ﹣33.35℃ |
(4)图中所标出的①②③的变化中,其中属于物理变化的过程是____,流程中能循环使用的物质是___(填名称)。
(5)写出N2、H2反应生成NH3的化学方程式_________。
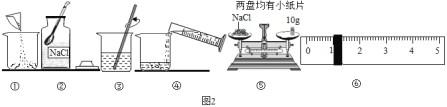
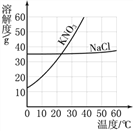
【题目】如下表中数据为氯化钠和硝酸钾在不同温度时的溶解度,如图所示是用其中一种物质所做的实验。下列分析正确的是( )

温度(℃) | 10 | 20 | 30 | 40 | |
溶解度/g | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 |
NaCl | 35.8 | 36.0 | 36.3 | 36.6 | |
A. 实验中加入的物质R是氯化钠 B. ④中t的取值范围在30~40之间
C. ③中的溶液可能是饱和溶液 D. ④中溶液的溶质质量分数可能比②中的大