题目内容
化学课上,老师提供信息“10gCuO用氢气还原一段时间后,称得残留固体质量为8.4g”,要求学生编制成化学计算题并求解.现摘取部分学生自编自解题中所设未知量的求解表达式,请你参照示例(1)在相关表达式右边框线上用文字简述x表示什么?
(1)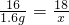 ,x=
,x=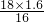 g,示例:________,
g,示例:________,
(2)x=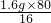 +10g×100%,________,
+10g×100%,________,
(3)x=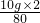 -
-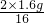 ,________.
,________.
(1)根据化学方程式:CuO+H2  Cu+H2O 固体质量减少
Cu+H2O 固体质量减少
18 16
x 10 g-8.4 g=1.6 g
可得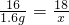 ,x=
,x=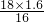 g,由此可知x表示反应后生成水的质量;
g,由此可知x表示反应后生成水的质量;
故答案为:表示反应后生成水的质量;
(2)根据化学方程式:CuO+H2 Cu+H2O 固体质量减少
Cu+H2O 固体质量减少
80 16
y 10 g-8.4 g=1.6 g
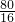 =
=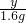 y=
y=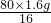 由此可知y为参加反应的CuO的质量,
由此可知y为参加反应的CuO的质量,
所以 x=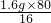 ÷10g×100%,则表示参加反应的CuO的质量分数;
÷10g×100%,则表示参加反应的CuO的质量分数;
故答案为:X表示原CuO中已分解的百分率;
(3)根据化学方程式:CuO+H2 Cu+H2O 固体质量减少
Cu+H2O 固体质量减少
80 2 16
10 z 10g-8.4g=1.6g
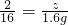 z=
z=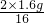 ,因此z表示当残留固体质量为8.4 g时,参加反应的H2的质量,
,因此z表示当残留固体质量为8.4 g时,参加反应的H2的质量,
同理可得10gCuO完全反应所需用氢气的质量为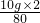 ,
,
所以x=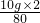 -
-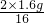 ,x表示理论上将剩余CuO全部还原成Cu还需H2的质量;
,x表示理论上将剩余CuO全部还原成Cu还需H2的质量;
故答案为:X表示理论上将剩余CuO全部还原成Cu还需H2的质量.
分析:根据反应化学方程式及参与反应的物质进行分析解答本题.
点评:误区:①因为反应没有完全进行,10g、8.4g都不是参加反应的物质的质量.②反应中还有H2进入,所以不能把10g-8.4g=1.6g当成H2O的质量进行.③化学方程式是反应中数据计算的基础,如果不列方程式,只对计算式进行分析,难度会很大.
通常情况下的化学计算是考生设出未知数,然后进行求解.本题打破常规解题方法,给出解题过程,然学生寻求未知数的含义,对考查学生的理解能力很有帮助.
 Cu+H2O 固体质量减少
Cu+H2O 固体质量减少 18 16
x 10 g-8.4 g=1.6 g
可得
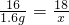 ,x=
,x=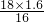 g,由此可知x表示反应后生成水的质量;
g,由此可知x表示反应后生成水的质量;故答案为:表示反应后生成水的质量;
(2)根据化学方程式:CuO+H2
 Cu+H2O 固体质量减少
Cu+H2O 固体质量减少 80 16
y 10 g-8.4 g=1.6 g
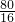 =
=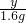 y=
y=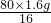 由此可知y为参加反应的CuO的质量,
由此可知y为参加反应的CuO的质量,所以 x=
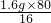 ÷10g×100%,则表示参加反应的CuO的质量分数;
÷10g×100%,则表示参加反应的CuO的质量分数; 故答案为:X表示原CuO中已分解的百分率;
(3)根据化学方程式:CuO+H2
 Cu+H2O 固体质量减少
Cu+H2O 固体质量减少 80 2 16
10 z 10g-8.4g=1.6g
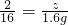 z=
z=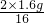 ,因此z表示当残留固体质量为8.4 g时,参加反应的H2的质量,
,因此z表示当残留固体质量为8.4 g时,参加反应的H2的质量,同理可得10gCuO完全反应所需用氢气的质量为
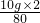 ,
,所以x=
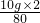 -
-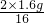 ,x表示理论上将剩余CuO全部还原成Cu还需H2的质量;
,x表示理论上将剩余CuO全部还原成Cu还需H2的质量;故答案为:X表示理论上将剩余CuO全部还原成Cu还需H2的质量.
分析:根据反应化学方程式及参与反应的物质进行分析解答本题.
点评:误区:①因为反应没有完全进行,10g、8.4g都不是参加反应的物质的质量.②反应中还有H2进入,所以不能把10g-8.4g=1.6g当成H2O的质量进行.③化学方程式是反应中数据计算的基础,如果不列方程式,只对计算式进行分析,难度会很大.
通常情况下的化学计算是考生设出未知数,然后进行求解.本题打破常规解题方法,给出解题过程,然学生寻求未知数的含义,对考查学生的理解能力很有帮助.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 ,x=
,x= g,示例:,
g,示例:, +10g×100%,,
+10g×100%,, -
- ,.
,.