题目内容
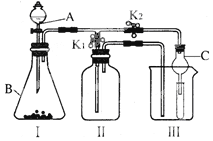
【题目】实验室常用的制备气体的装置如下图所示,请根据要求完成问题.
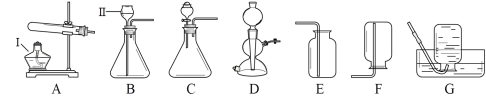
写出仪器名称:Ⅰ ;Ⅱ ;
② 用氯酸钾和二氧化锰的混合物制取较干燥的氧气可选择的发生和收集装置是 (填装置编号);
③ 制取下列气体可以用启普发生器作为发生装置的是 .
a.双氧水与二氧化锰粉末混合制取氧气
b.实验室制取二氧化碳
c.用锌粒和稀硫酸制取氢气
④ 要制取0.02mol氢气,至少需要多少克锌粒和足量稀硫酸反应?(请根据化学方程式列式计算) .
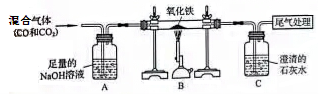
⑤ 从废旧干电池中回收的MnO2含有C,为得到纯净的MnO2并测定MnO2的含量,取该混合物用下图装置进行实验(夹持装置已略去).

Ⅰ.实验中,用双氧水与二氧化锰混合制取氧气的化学方程式是 ;为得到平稳的氧气流选用的发生装置是 (选填A~G的装置编号).
Ⅱ.下列数据中可以用来计算样品中MnO2的含量的是 .(假设每步反应均完全且称量准确)
a.反应前后氧气发生装置的质量
b.反应前后装置Ⅰ中固体的质量
c.反应前后装置Ⅱ中固体的质量
d.反应前后装置Ⅲ中固体的质量
【答案】①酒精灯 长颈漏斗 ②AE ③bc ④1.3g
⑤Ⅰ、2H2O2![]() 2H2O+ O2↑ C Ⅱ、b
2H2O+ O2↑ C Ⅱ、b
【解析】
试题分析:①常见仪器的识记:酒精灯、长颈漏斗
②气体发生装置的选择依据:反应物的状态和反应条件,用氯酸钾和二氧化锰的混合物需要加热,属于固固加热型,故发生装置选择A;收集装置的选择依据:气体的密度和溶解性,要制取较干燥的氧气,宜采用向上排空气法,故收集装置选E
③启普发生器的使用范围:颗粒状固体和液体再常温下反应产生气体,故a、双氧水与二氧化锰粉末混合制取氧气,不能采用启普发生器,因为二氧化锰是粉末;故选bc
④根据化学方程式:Zn + H2SO4 → ZnSO4 + H2↑中Zn与H2的物质的量的关系
解:设需要锌粒x mol
Zn + H2SO4 → ZnSO4 + H2↑
1 1
x 0.02
1:x=1:0.02
x=0.02(mol)
锌的质量:0.02mol×65g/mol=1.3g
⑤Ⅰ、用双氧水与二氧化锰混合制取氧气的化学方程式是:2H2O2![]() 2H2O+ O2↑;为得到平稳的氧气流选用的发生装置是C,通过分液漏斗控制滴加液体的速率,从而控制反应速率
2H2O+ O2↑;为得到平稳的氧气流选用的发生装置是C,通过分液漏斗控制滴加液体的速率,从而控制反应速率
Ⅱ、通过实验装置可知,该实验原理:C+O2![]() CO2,而二氧化锰不会与氧气反应,故反应前后装置Ⅰ中固体的质量,即为参加反应的碳质量,进而可计算出样品中MnO2的含量,故选b,
CO2,而二氧化锰不会与氧气反应,故反应前后装置Ⅰ中固体的质量,即为参加反应的碳质量,进而可计算出样品中MnO2的含量,故选b,