题目内容
【题目】请从33-A或33-B两题中任选一个作答,若两题均作答,按33-A计分。
33-A | 33-B |
|
|
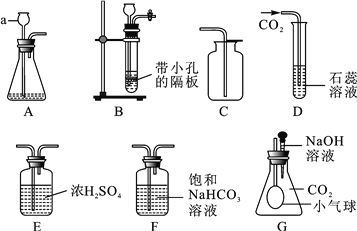
(1)实验室用高锰酸钾制取氧气的化学方程式为_____。 (2)证明收集到的气体为氧气的方法是_____。 | (1)用大理石和稀盐酸制取二氧化碳的化学方程式为_____。 (2)检验二氧化碳已经收集满的方法 是_____。 |
【答案】 2KMnO4![]() K2MnO4+MnO2+O2↑ 将带火星的木条伸入集气瓶,若木条复燃,说明是氧气 CaCO3+2HCl=CaCl2+H2O+CO2↑ 用燃着的木条放在集气瓶口,若木条熄灭,说明集满
K2MnO4+MnO2+O2↑ 将带火星的木条伸入集气瓶,若木条复燃,说明是氧气 CaCO3+2HCl=CaCl2+H2O+CO2↑ 用燃着的木条放在集气瓶口,若木条熄灭,说明集满
【解析】33-A(1)根据高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气解答;(2)用带火星的木条检验氧气;33-B(1)根据碳酸钙和稀盐酸在常温下反应生成氯化钙、水喝二氧化碳解答;(2)根据用燃着的木条检验二氧化碳是否收集满解答。33-A(1)根据高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4△K2MnO4+MnO2+O2↑;(2)证明收集到的气体为氧气的方法是将带火星的木条伸入集气瓶,若木条复燃,说明是氧气;33-B(1)碳酸钙和稀盐酸在常温下反应生成氯化钙、水喝二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)检验二氧化碳已经收集满的方法是用燃着的木条放在集气瓶口,若木条熄灭,说明集满。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示溶液),他们对此产生了兴趣。
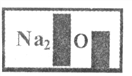
[提出问题]这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种。为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是______。
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是_______。
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验。
[设计实验]
实验操作 | 实验现象 |
取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 |
[实验结论]
(3) 该瓶无色溶液是_______。生成白色沉淀过程的化学方程式是________。
[实验反思]
(4)小强认为上述设计实验还可简化,仍能达到目的。小强的实验操作是______。经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐。简述实验操作和现象____________。