题目内容
下列各组离子能在溶液中大量共存的是( )
| A、Na+、Mg2+、Cl-、OH- |
| B、H+、Ca2+、CO32-、NO3- |
| C、Cu2+、K+、SO42-、NO3- |
| D、Na+、HCO3-、OH-、Ca2+ |
考点:离子或物质的共存问题
专题:物质的分离、除杂、提纯与共存问题
分析:根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可
解答:解:A、Mg2+与OH-反应生成氢氧化镁沉淀而不能大量共存,故A错误;
B.CO32-与H+、Ca2+反应分别产生水、二氧化碳和碳酸钙沉淀而不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.HCO3-与OH-反应而不能大量共存,故D错误.
故选C.
B.CO32-与H+、Ca2+反应分别产生水、二氧化碳和碳酸钙沉淀而不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.HCO3-与OH-反应而不能大量共存,故D错误.
故选C.
点评:本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
黑火药是我国的四大发明之一,距今己有一千多年的历史.黑火药爆炸的原理可用下式表示:2KNO3+3C+S
K2S+N2↑+3X↑,根据质量守恒定律,推断X的化学式(分子式)为( )
| 点燃 |
| A、CO |
| B、CO2 |
| C、NO |
| D、SO2 |
金秋十月,人们站在桂花树旁常能闻到怡人的桂花香,这一现象说明了( )
| A、分子很大 |
| B、分子分裂成原子 |
| C、分子在不断地运动 |
| D、分子之间有间隔 |
自来水生产中常通适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸.市场上有些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售.为辨别真伪,可用下列一种化学试剂来鉴别,该试剂是( )
| A、酚酞试液 |
| B、氯化钡溶液 |
| C、氢氧化钠溶液 |
| D、硝酸银溶液 |
将质量相等、百分比浓度相同的氢氧化钠溶液和盐酸混合,再滴入石蕊试液,溶液呈现的颜色是( )
| A、红色 | B、蓝色 | C、紫色 | D、无色 |
下列各组概念中,前者一定包含后者的是( )
| A、纯净物混合物 |
| B、化学变化物理变化 |
| C、氧化反应化合反应 |
| D、化学反应分解反应 |
将100g 10%的NaOH溶液与100g 10%的稀硫酸充分混合,下列判断正确的是( )
| A、最后溶液呈中性 |
| B、最后溶液中只有硫酸钠一种溶质 |
| C、最后溶液滴入紫色的石蕊溶液呈蓝色 |
| D、最后溶液的质量小于200g |
用数轴表示某些化学知识直观、简明、易记.下列数轴表示错误的是( )
A、银、铜、铁的金属活动性强弱: |
B、根据铁的含碳量,将其分成生铁和钢: |
C、物质形成溶液的pH: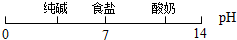 |
D、氮气、及其化合物与化合价的关系: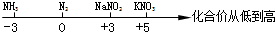 |