题目内容
现有铁和氧化铁的混合物10.0 g,用一氧化碳充分还原后得到铁
7.6 g,试计算10.0 g混合物中氧化铁的质量分数。
【答案】
80%
【解析】设原混合物中含铁的质量为x。
Fe2O3+3CO=2Fe+3CO2
160???????? 112
10.0 g-x? 7.6 g-x
160∶112=(10.0 g-x)∶(7.6 g-x),
解得:x=2.0 g
混合物中含氧化铁的质量分数为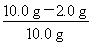 ×100%=80%。
×100%=80%。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目