题目内容
【题目】Ca(OH)2变质得到Ca(OH)2和CaCO3的混合物。李琳同学设计了如下图的实验装置来测定CaCO3的含量,她用气密性良好的装置装上药品并通一会儿氮气后关闭止水夹,再打开分液漏斗活塞。提示:碱石灰(可以吸收CO2和H2O)浓硫酸均足量,稀盐酸不考虑其挥发性。
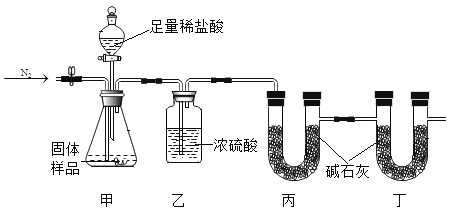
(1)通入N2的原因之一是N2的化学性质_____(填活泼或者不活泼)。
(2)甲装置中发生中和反应的化学方程式为_____。
(3)浓硫酸的作用是_____。
(4)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。
①另一个物理量为_____(填序号)。
A 滴下的稀盐酸质量 B 反应前后乙装置增加的质量
C 反应前后丙装置增加的质量 D 反应前后丁装置增加的质量
②若去掉丁装置,测得CaCO3含量_____(填“偏高”、“偏低”或“不变")。
③甲装置中反应结束后打开止水夹再通入一会儿N2的目的是_____。
【答案】不活泼 Ca(OH)2+2HCl=CaCl2+2H2O 干燥二氧化碳(或除去二氧化碳中的水蒸气)(合理表述即可) C 偏高 排出甲、乙装置及连接导管中的二氧化碳气体,使其被丙装置内碱石灰吸收,实验结果更加准确。
【解析】
(1)氮气化学性质不活泼,可以赶走装置内空气防止空气中二氧化碳对实验的干扰;
(2)稀盐酸与氢氧化钙发生复分解反应:Ca(OH)2+2HCl=CaCl2+2H2O;
(3)浓硫酸具有吸水性,可以干燥二氧化碳(或除去二氧化碳中的水蒸气);
(4)①测定CaCO3的含量需要测定样品的质量和反应后生成二氧化碳的质量,即反应前后丙装置增加的质量。故选C;
②去掉丁装置,空气中的二氧化碳和水汽会被丙装置吸收,导致质量增加,使测得CaCO3含量偏高;
③甲装置中反应结束后打开止水夹再通入一会儿N2可以使反应后生成二氧化碳完全被丙装置内碱石灰吸收,实验结果更加准确。

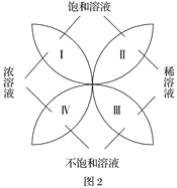
【题目】下表提供的四组物质符合图示相连物质间在一定条件下可以发生反应的是
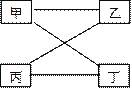
甲 | 乙 | 丙 | 丁 | |
A | CO | O2 | H2SO4 | CuO |
B | Mg | HCl | CuSO4 | NaOH |
C | KOH | SO3 | NaOH | CuSO4 |
D | Na2CO3 | Ca(OH)2 | HCl | CaCl2 |
【题目】金属在生产和生活中应用广泛。请回答下列问题。
(1)生活中常用铁锅做饭,主要利用了铁的_____性。
(2)厨房中铁锅容易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法_____。
(3)铝合金制造的飞机外壳,具有轻量化、能抗击强大气流的冲击、耐受水雾和雨雪侵蚀等特点。这是利用了铝合金的_____、_____等优点(写出两条即可)。
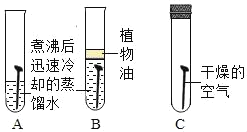
(4)某研究小组为探究铁、铜、锰(Mn)的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用 5%的盐酸体积相同)。
(实验记录与分析)
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | 立即产生气泡,速率较慢 | 无明显现象 | 立即产生气泡,速率较快 |
实验结论 | 铁、铜、锰的金属活动性顺序由强到弱为______>______>_____ | ||
写出实验一试管中铁和盐酸发生反应的化学方程式_________________________________________________________________。