题目内容
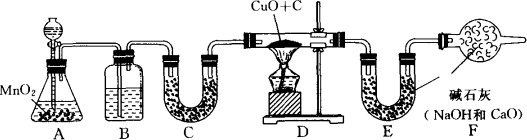
为了测定一包均匀混合的铜粉和木炭粉的混合物中铜的质量分数,某化学课外小组的同学设计了如图所示的实验(实验装置的气密性良好,图中铁架台等仪器均已略去).他们利用了30%的双氧水与二氧化锰作用制取实验中所需的氧气,反应的化学方程式是:2H2O2![]() 2H2O+O2↑,请回答下列有关问题:
2H2O+O2↑,请回答下列有关问题:
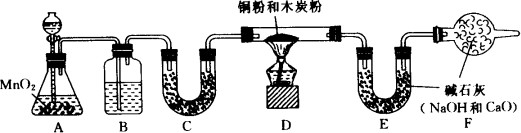
(1)B装置中盛放的试剂是________,作用是________;C装置中盛放的试剂是________,作用是________.
(2)F装置的作用是________.
(3)已知硬质玻璃管中装有铜粉和木炭粉的混合物6 g,反应完全后(氧气过量),停止加热并冷却至室温,称得E装置增加了3.3 g,则样品中铜的质量分数是________%.
(4)实验完毕后,老师让同学们自我评价,如果没有B、C、F装置,实验所测得的铜的质量分数将________(填“偏大”或“偏小”).
答案:

练习册系列答案
相关题目