题目内容
【题目】碳元素是组成许多物质的基本元素。
(1)下列含碳元素的物质中,能引起温室效应的是______(填字母序号)。
A.一氧化碳 B.乙醇(C2H5OH ) C.二氧化碳
(2)化石燃料主要包括煤、_______和_______,它们都含有碳元素。
(3)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰( MnCO3),其中锰元素的化合价为________ 。
(4)在 440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为 _________________________________ 。
(5)“碳海绵”是已知最轻的固体材料(如下图所示),由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是 ________ (填字母序号)。

A.具有吸附性 B.可重复使用 C.可处理海上石油泄漏
【答案】C 石油 天然气 +2 4Na+3CO2![]() C+2Na2CO3 A、B、C
C+2Na2CO3 A、B、C
【解析】
(1)一氧化碳有毒,是空气污染物,但不能引起温室效应;酒精是液体,不会引起温室效应;二氧化碳是温室气体,能引起温室效应;(2)三大化石燃料:煤、石油、天然气;天然气主要成分是甲烷;(3)化合物中元素的化合价代数和为零,在MnCO3中碳酸根化合价是-2价,锰元素化合价是+2价;(4)反应物是钠和二氧化碳,生成物是碳和碳酸钠,反应条件是440℃和高压,用观察法配平,所以方程式是:3CO2+4Na![]() 2Na2CO3+C;(5)“碳海绵”具有多孔结构,对石油有很强的吸附能力(不吸水),所以具有吸附性,将吸入的石油挤出后仍可恢复原状,所以可重复使用;它对石油有很强的吸附能力,所以可处理海上石油泄漏。故选A、B、C。
2Na2CO3+C;(5)“碳海绵”具有多孔结构,对石油有很强的吸附能力(不吸水),所以具有吸附性,将吸入的石油挤出后仍可恢复原状,所以可重复使用;它对石油有很强的吸附能力,所以可处理海上石油泄漏。故选A、B、C。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
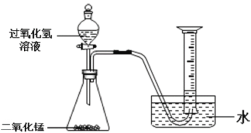
(1)如上图所示进行实验,过氧化氢分解的化学方程式为______。
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响。
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度 % | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40 min | 40 min | 40 min |
由此得出的结论是______。
Ⅱ.腐蚀性
(查阅资料)H2O2溶液有腐蚀性。
(进行实验)
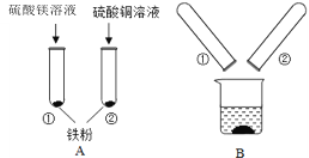
同学们用铜片设计实验验证H2O2溶液的腐蚀性。(各组实验中H2O2溶液和稀硫酸所用浓度均相同)
将铜片分别浸泡在3种溶液中进行实验,如下表。

(解释与结论)
(4)实验①的作用是______。
(5)能说明铜片被腐蚀与H2O2溶液和稀硫酸均有关的实验组是______。
(6)铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu + H2O2+ H2SO4=== CuSO4 +□_______