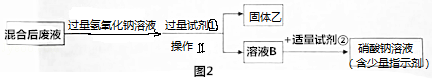
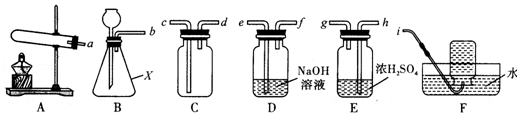
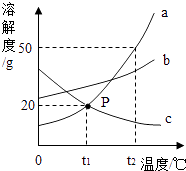
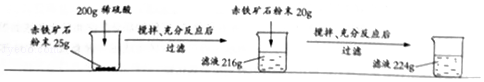
题目内容
【题目】某同学要用含CaCO380%的大理石与足量的稀盐酸反应制备1000mL标准状况下的二氧化碳气体.己知标准状况下的二氧化碳气体的密度为:1.98g/L.假设大理石中的杂质不与稀盐酸反应,计算该同学最少需要准备多少克大理石.
【答案】解:1000mL=1L 设需要含碳酸钙80%的大理石的质量为x
CaCO3+2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 111 | 44 |
x×80% | 1L×1.98g/L |
![]()
x=5.625g
答:该同学最少需要准备5.625克大理石
【解析】实验室利用碳酸钙与盐酸反应制取二氧化碳气体,根据反应的化学方程式可确定反应中碳酸钙与二氧化碳的质量关系,利用这种质量关系,由二氧化碳质量可求得碳酸钙质量.
【考点精析】利用根据化学反应方程式的计算对题目进行判断即可得到答案,需要熟知各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目