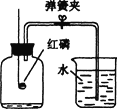
题目内容
【题目】在CO和CO2的混合气体中,氧元素的质量分数是64%,将该气体5g通过足量的灼热的CuO粉末,完全反应后,气体通过足量的澄清石灰水得到白色沉淀的质量是( )
A. 5g B. 6.7g C. 15g D. 20g
【答案】C
【解析】
解法1:
设5g混合气体中一氧化碳的质量为m,则二氧化碳质量为5g-m,根据题意得:
m×![]() ×100%+(5g-m)×
×100%+(5g-m)×![]() ×100%=5g×64%,m=2.8g;
×100%=5g×64%,m=2.8g;
设2.8g一氧化碳与氧化铜完全反应生成二氧化碳的质量为x,
CO+CuO![]() Cu+CO2
Cu+CO2
28 44
2.8g x
![]()
x=4.4g,
10g混合气体通过足量的灼热的氧化铜粉末后,二氧化碳气体质量=4.4g+(5g-2.8g)=6.6g,设生成沉淀的质量为y,
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
6.6g y
![]()
y=15g。故选C。
解法二:(巧妙计算)由于碳元素最终全部在碳酸钙中,所以可以用关系式法直接计算;碳元素的质量为5g×(1-64%)=1.8g,设生成的碳酸钙的质量为x,
则有C~~~CaCO3
12 100
1.8g x
![]()
x=15g;
或者由于碳元素最终全部在碳酸钙中,所以可以用碳酸钙中碳元素的质量分数直接计算。
碳元素的质量为5g×(1-64%)=1.8g;由于碳酸钙中碳元素的质量分数为:![]() ×100%=12%,则1.8g碳元素对应的碳酸钙的质量为:
×100%=12%,则1.8g碳元素对应的碳酸钙的质量为:![]() =15g。故选:C。
=15g。故选:C。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】现有硫酸钠和氯化钠的固体混合物30g,加316.6g水使之全部溶解,将300g氯化钡溶液分三次加入该溶液中,实验数据记录如下表:
第1次 | 第2次 | 第3次 | |
加入氯化钡溶液质量/g | 100 | 100 | 100 |
生成沉淀的质量/g | 23.3 | m | 46.6 |
(1)表中m的数值是_______。
(2)原固体混合物中硫酸钠的质量分数是多少_______?(计算结果精确到0.1%)
(3)恰好完全反应时,所得溶液中溶质的质量分数的多少______?
【题目】一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料,合成一系列化工原料和燃料的化学.
(1)煤和高温水蒸气反应可以生成CO和H2 , 反应的化学方程式为________.
(2)天然气的重整可以得到合成气.其微观过程示意图如下所示: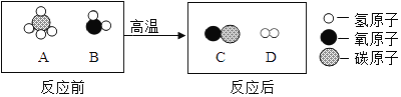
上述物质中,生成物C与D的质量比为________.
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质.仅以合成气为原料不可能得到的物质是_______(填字母序号).
A. 草酸(H2C2O4) B. 甲醇(CH3OH) C. 尿素[CO(NH2)2]
(4)根据下表回答相关问题.
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 (g/100g 水) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
①如表中两种物质的溶解度相等的温度范围是在________℃.
②20℃时,硝酸钾的溶解度是________,该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是________.要进一步提高该溶液的溶质质量分数,可进行的操作是________.
【题目】南海是中国四大海域中最大、最深、自然资源最为丰富的海域,南海不但资源丰富,还是亚太地区海运的“咽喉要道”,这里有世界上最繁忙的航线,因此引起周边国家的窥视.
(1)海水属于 (填“纯净物”或“混合物”);海水晒盐属于混合物分离操作的方法是 .(填序号)
A.蒸馏 | B.蒸发 | C.过滤 | D.沉淀 |
(2)南海天然气资源丰富,用天然气代替燃煤是防止空气污染的措施之﹣.请写出天然气燃烧的化学方程式: .
(3)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残损严重,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序是 .
(4)生铁和钢是世界上用量最大的 (填“金属材料”或“合成材料”);炼铁的原理是利用一氧化碳与氧化铁反应,反应的化学方程式为 ;写出防止铁生锈的一种方法是 .