题目内容
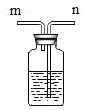
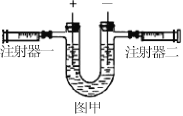
【题目】利用如图1装置,小卫设计并实施了下列实验,(压强传感器用于测量抽滤瓶内压强变化:各数据均于同温下测定获得)
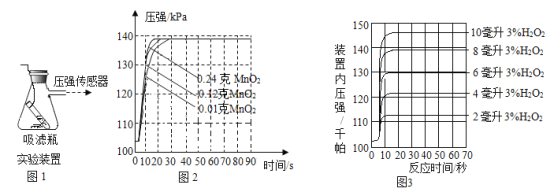
实验Ⅰ:再小试管中加入8mL溶质质量分数为3%的双氧水(ρ=1g/mL),在抽滤瓶中分别加入不同质量的MnO2,使其反应并启动传感器,记录容器内压强变化于图2中.
实验Ⅱ:在抽滤瓶中加入0.1g MnO2,在小试管中分别加入不同体积溶质质量分数为3%的双氧水,使其反应并启动传感器,记录容器内压强变化于图3中.
请根据以上实验回答下列问题:
(1)使容器内压强增大的反应的化学方程式:_____________________;
(2)根据图2可发现,该实验条件下,30s内催化分解8mL溶质质量分数为3%的双氧水,MnO2的最小用量为______________g;
(3)根据图3可发现,0.1g MnO2至少能快速催化分解__________g过氧化氢;
(4)根据图2与图3可发现,MnO2的用量总体上与O2产量_____________(填“正相关”、“不相关”或“负相关”),根据图3还可发现,该试验中,O2产量总体上与双氧水用量是___________(填“正比”或“反比”);
(5)下列因素中,与本实验所测数据的精确度有关的是__________ 。
A反应容器的气密性 B称量MnO2质量的精准度 C量取双氧水体积的精准度
【答案】2H2O2![]() 2H2O+O2↑ 0.01g 0.3g 不相关 正比 ABC
2H2O+O2↑ 0.01g 0.3g 不相关 正比 ABC
【解析】
(1)容器内压强增大,是因为过氧化氢在二氧化锰催化作用下分解生成了氧气和水,反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)根据图2可发现,实验条件下,30s内催化分解8mL溶质质量分数为3%的双氧水,MnO2的最小用量为0.01g;
(3)根据图3可发现,0.1g MnO2至少能快速催化分解10mL的过氧化氢溶液,10mL过氧化氢溶液中过氧化氢的质量为:1g/mL×10mL×3%=0.3g;
(4)根据图2与图3可发现,MnO2的用量总体上与O2产量不相关,根据图3还可发现,该试验中,O2产量总体上与双氧水用量是成正比;
(5)如果反应容器的气密性不好,称量MnO2质量不准确,量取双氧水体积不准确,都能够影响实验所测数据的精确度。故选ABC。

【题目】小金为了探究温度对过氧化氢分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
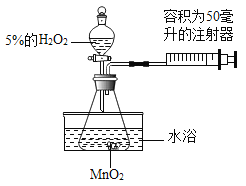
实验1 | 实验2 | |
二氧化锰的质量/克 | 0.5 | 0.5 |
5%的过氧化氢的体积/毫升 | 40 | 待填 |
水浴温度/℃ | 20 | 80 |
(1)实验2中应加入5%过氧化氢____________毫升;
(2)在两次实验中,可通过_____________________来比较过氧化氢分解反应速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有__________________;