题目内容
向一定体积的NaOH稀溶液中逐滴滴加稀盐酸,溶液pH变化的曲线合理的是( )
A、 |
B、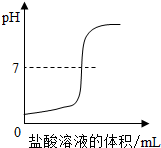 |
C、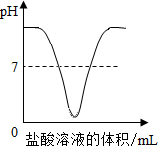 盐酸溶液的体积/mL |
D、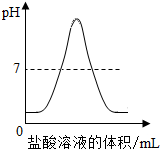 盐酸溶液的体积/mL |
考点:中和反应及其应用,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:向一定体积的NaOH稀溶液中逐滴滴加稀盐酸,溶液pH的变化曲线的变化趋势为:原溶液氢氧化钠溶液显碱性,pH值大于7;把盐酸溶液逐滴滴入,与氢氧化钠溶液反应,中和至恰好完全反应,pH值等于7;再滴入盐酸,盐酸过量,溶液呈酸性,pH值小于7.
解答:解:氢氧化钠溶液显碱性,碱性溶液的pH大于7;向NaOH溶液中不断滴加盐酸溶液时,盐酸与氢氧化钠发生中和反应生成氯化钠和水,生成的氯化钠溶液呈中性,由于氢氧化钠减少,所以溶液的pH不断减小,中和至恰好完全反应,溶液呈中性,溶液的pH等于7;再滴加稀盐酸,盐酸过量,溶液显酸性,溶液的pH小于7.
故A图象溶液pH变化的曲线合理.
答案:A.
故A图象溶液pH变化的曲线合理.
答案:A.
点评:本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
通常情况下,下列选项中的两种物质之间不能发生化学反应的是( )
| A、稀HNO3与Mg(OH)2 |
| B、CuO与稀H2SO4 |
| C、Cu与NaNO3溶液 |
| D、Na2CO3溶液与CaCl2溶液 |
胃溃疡严重的病人胃酸过多,可服用含有能跟盐酸其反应的物质成分的胃药,以减少胃中盐酸的含量而又不造成胃穿孔.下列物质中,最适宜作为胃药成分的是( )
| A、小苏打 | B、氢氧化铝 |
| C、氢氧化钠 | D、氢氧化钙 |
下列物质属于纯净物的是( )
| A、冰水混合物 |
| B、澄清石灰水 |
| C、石 灰石 |
| D、高锰酸钾制氧气后的剩余固体 |
下列说法正确的是( )
| A、pH等于8的溶液一定是碱的溶液 |
| B、若某物质中只含有一种元素,则该物质一定是单质 |
| C、向某固体中滴加稀盐酸,有气泡产生,则固体中一定含有碳酸根粒子 |
| D、一定温度下,某溶质的不饱和溶液变为饱和溶液,其溶质质量分数一定变大 |
下列说法属于化学性质的是( )
A、 能导电 |
B、 硬度最大 |
C、 常温下呈气态 |
D、 会生锈 |
下列说法中错误的是( )
| A、人呼出的气体中水蒸气的含量比空气中水蒸气的含量大 |
| B、绿色化学的核心是利用化学原理从源头消除污染 |
| C、铁生锈包含缓慢氧化反应 |
| D、将带火星的木条放入集气瓶内,木条复燃,证明收集满了 |