题目内容
胃溃疡严重的病人胃酸过多,可服用含有能跟盐酸其反应的物质成分的胃药,以减少胃中盐酸的含量而又不造成胃穿孔.下列物质中,最适宜作为胃药成分的是( )
| A、小苏打 | B、氢氧化铝 |
| C、氢氧化钠 | D、氢氧化钙 |
考点:常见碱的特性和用途,常用盐的用途
专题:常见的碱 碱的通性
分析:胃药的成分必须是能跟盐酸反应的物质,以减少胃中盐酸的含量,可以推测胃药的主要成分应该是碱性物质,而NaHCO3水溶液呈碱性,但与盐酸反应会放出二氧化碳加重病情,可能造成胃穿孔;氢氧化钠具有强烈的腐蚀性;Ca(OH)2是一种碱,具有较强的腐蚀性,不宜做胃药;据此进行分析判断.
解答:解:A、小苏打的水溶液呈碱性,但与盐酸反应生成二氧化碳气体,造成病情加重,对于患胃溃疡的病人,反应产生的二氧化碳气体会造成胃部气胀,易造成胃穿孔,故选项错误.
B、氢氧化铝是不溶性的碱,能中和胃酸而减少胃中盐酸的含量,最适宜作为胃药成分,故选项正确.
C、氢氧化钠具有强烈的腐蚀性,不适宜作为胃药成分,故选项错误.
D、Ca(OH)2是一种碱,具有较强的腐蚀性,不适宜作为胃药成分,故选项错误.
故选:B.
B、氢氧化铝是不溶性的碱,能中和胃酸而减少胃中盐酸的含量,最适宜作为胃药成分,故选项正确.
C、氢氧化钠具有强烈的腐蚀性,不适宜作为胃药成分,故选项错误.
D、Ca(OH)2是一种碱,具有较强的腐蚀性,不适宜作为胃药成分,故选项错误.
故选:B.
点评:本题难度不大,考查酸的化学性质,掌握酸的化学性质、常见碱的特性与用途是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
鱼油中富含的DHA(C22H32O2)是大脑细胞形成和发育不可缺少的物质,下列关于DHA的叙述中正确的是( )
| A、DHA由碳、氢、氧三种原子构成 |
| B、DHA中碳、氢、氧三种元素的质量比为33﹕8﹕4 |
| C、DHA由三种元素组成 |
| D、DHA中氢元素的质量分数最大 |
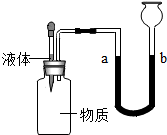 下列各组物质按如图所示装置进行实验,当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化.若a处液面降低,则符合此现象的物质组合的是( )
下列各组物质按如图所示装置进行实验,当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化.若a处液面降低,则符合此现象的物质组合的是( )| 选项 | 液体 | 物质 |
| A | 氢氧化钠溶液 | 二氧化碳 |
| B | 水 | 氯化钠 |
| C | 水 | 硝酸铵 |
| D | 过氧化氢溶液 | 二氧化锰 |
| A、A | B、B | C、C | D、D |
元素的化学性质主要决定于原子中的( )
| A、质子数和中子数 |
| B、电子总数 |
| C、最外层电子数 |
| D、中子数 |
12gFe2O3和CuO的混合物与足量CO充分反应后固体减轻3.2g,原混合物中Fe2O3和CuO的质量比是( )
| A、1:1 | B、2:1 |
| C、3:1 | D、3:2 |
向一定体积的NaOH稀溶液中逐滴滴加稀盐酸,溶液pH变化的曲线合理的是( )
A、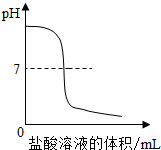 |
B、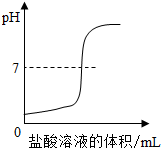 |
C、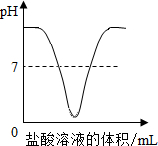 盐酸溶液的体积/mL |
D、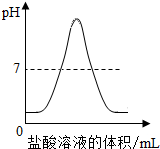 盐酸溶液的体积/mL |
在密闭容器中盛有6克碳和12克氧气,加热使它们充分反应后,最后容器内的气体应该是( )
| A、CO2 |
| B、CO |
| C、CO2和CO |
| D、CO2和O2 |
学完金属的化学性质后,化学兴趣小组的同学们有下列描述或判断,其中正确的是( )
| A、金属钾能与硫酸锌溶液发生化学反应得到金属锌 |
| B、金属铁与硫酸溶液反应后所得溶液的质量比原溶液的质量增大 |
| C、在空气中铝比铁更耐腐蚀,说明铁的活动性比铝强 |
| D、金属铜与氯化银反应得到金属银 |