题目内容
【题目】如图中的A~H都是初中化学中常见的物质,已知A、B都是黑色固体,D为红色固体单质,F为红棕色固体氧化物,它们之间的转化关系如图所示,请推断出各物质后回答下列问题: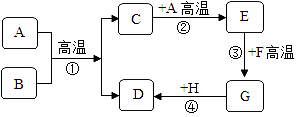
(1)写出物质A的化学式;
(2)写出物质E的用涂;
(3)转化过程①可用化学方程式表示为;
(4)已知转化过程④在常温下就能进行,该化学反应的基本类型为 .
【答案】
(1)C
(2)作燃料(或冶炼金属)
(3)C+2CuO ![]() 2Cu+CO2↑
2Cu+CO2↑
(4)置换反应
【解析】根据所学知识和题中信息知,A、B都是黑色固体,D为红色固体单质,F为红棕色固体氧化物。A是碳,B是氧化铜。C是二氧化碳,D是铜。E是一氧化碳,F是氧化铁。G是铁,H是可溶性铜盐。(1)物质A的化学式是. C 。﹙ 2)物质E具有可燃性,还原性。用途是作燃料(或冶炼金属)。(3)转化过程①可用化学方程式表示为C+2CuO ![]() 2Cu+CO2↑。(4)已知转化过程④在常温下就能进行,该化学反应的基本类型为置换反应。
2Cu+CO2↑。(4)已知转化过程④在常温下就能进行,该化学反应的基本类型为置换反应。
故答案为:C;作燃料(或冶炼金属);C+2CuO ![]() 2Cu+CO2↑;置换反应。
2Cu+CO2↑;置换反应。
推断题关键是根据已知信息找出对应的物质,再根据物质写出相关的化学方程式。反应类型的判断,其中反应类型共分为四大类,可简单归纳为:化合反应:多合一;分解反应:一分多;置换反应:单化化单;复分解反应:相互交换价不变。

 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5 mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
实验序号 | 滴加CuSO4 溶液的量 | 实验现象 |
① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多。振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式_____________。
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下稳定,70 ℃~80 ℃时分解生成氧化铜。
Ⅱ.铜酸钠[Na2Cu(OH)4]溶液呈亮蓝色。
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应。
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液。
甲同学认为猜想Ⅰ不成立,理由是______________________________。
乙同学为验证猜想Ⅱ,进行了如下实验。
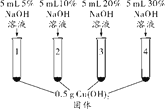
【进行实验】
实验操作 |
|
实验现象 | |
1号试管,…… | |
2号试管,蓝色固体不消失 | |
3号试管,蓝色固体减少 | |
4号试管,蓝色固体消失,得到亮蓝色溶液 |
【解释与结论】
(1)1号试管中现象为_________________________________。
(2)上述实验得出的结论是__________________________。
【反思与评价】
(1)进一步查阅资料可知,氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠,反应的化学方程式为__________________________。
(2)丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是____________________________。