题目内容
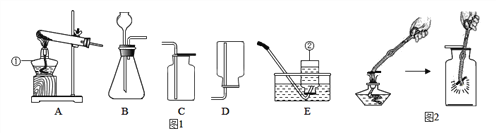
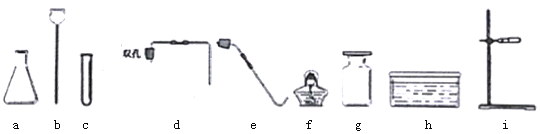
【题目】某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从图中选择装置进行了氧气的制备实验.
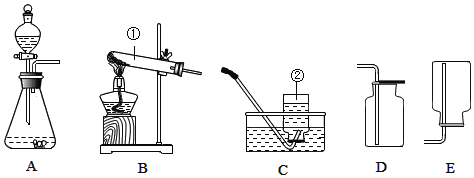
(1)写出下列序号仪器名称:①_____;②_____.
(2)甲同学从如图中选择A、D装置的组合制取氧气,反应的化学方程式为_____
(3)实验室若用高锰酸钾来制氧气,应选用的发生装置是_____(填序号),若用排水法收集氧气,必须等到_____才开始收集,收集完氧气后,发现水槽中的水变成了紫红色,分析产生该现象的是原因可能是_____
(4)用排水法收集实验室制得的氧气,结果不纯,原因可能是_____(答出一条即可)
(5)同学们称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,乙同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想I:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2;
猜想Ⅲ:反应生成的K2MnO4和MnO2分解都放出O2.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想_____错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论.该组同学选择的实验方法是_____.
【拓展延伸】实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快.请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?_____
【实验反思】通过以上实验探究,你对“实验制取氧气”还想探究的问题是_____.
【答案】 试管 集气瓶 2H2O2![]() H2O+O2↑ B 气泡连续均匀冒出时 试管口没有放一团棉花 集气瓶没有装满水 I和III 把带火星的木条伸入试管中,观察是否复燃 【答题空10】否,加入高锰酸钾后,高锰酸钾受热会分解生成氧气,而且产物二氧化锰是氯酸钾的催化剂,也会加快氯酸钾的分解速率,高锰酸钾不是氯酸钾分解的催化剂 氯酸钾分解的最低温度
H2O+O2↑ B 气泡连续均匀冒出时 试管口没有放一团棉花 集气瓶没有装满水 I和III 把带火星的木条伸入试管中,观察是否复燃 【答题空10】否,加入高锰酸钾后,高锰酸钾受热会分解生成氧气,而且产物二氧化锰是氯酸钾的催化剂,也会加快氯酸钾的分解速率,高锰酸钾不是氯酸钾分解的催化剂 氯酸钾分解的最低温度
【解析】(1)①仪器的名称是试管;②仪器的名称是集气瓶;(2)AD是固液不加热型装置,是用过氧化氢制取氧气,故反应方程式为2H2O2 MnO2 2H2O+O2↑;(3)实验室用高锰酸钾制取氧气时,反应的条件是加热,故选择固固加热型装置,选B装置;用排水法收集氧气时,要待气泡连续均匀冒出时才能收集,否则收集的气体中含有试管中的空气;水槽中变为紫红色可能是因为试管口没有放一团棉花,高锰酸钾通过导管进入到了水槽中;(4)用排水法收集氧气时,如集气瓶中有空气的话,会使收集的起不纯;(5)加热二氧化锰后质量不变说明二氧化锰没有分解,则猜想I和III是错误的;直接把带火星的木条伸入试管中,观察是否复燃,如复燃,则说明有氧气生成;高锰酸钾不是催化剂,而是加入高锰酸钾后,高锰酸钾受热会分解生成氧气,而且产物二氧化锰是氯酸钾的催化剂,也会加快氯酸钾的分解速率,故高锰酸钾不是氯酸钾分解的催化剂;氯酸钾分解的最低温度是多少,还有哪些物质可以做为氯酸钾反应的催化剂等,合理即可。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】下列实验方案与实验结论相对应的是
选项 | ① | ② | ③ | ④ |
方案 |
|
|
|
|
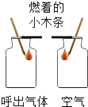
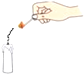
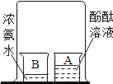
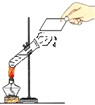
结论 | 比较呼出气体中CO2含量较空气中的多 | 说明白烟的成分不是二氧化碳 | 说明氨分子在不断地运动,而酚酞分子不运动 | 说明液态水与气态水可以相互转化 |
A. ①②④ B. ①④ C. ①②③④ D. ②④