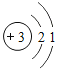题目内容
【题目】各种物质之间存在着某种联系。请分别选用“>”、“<” 、“=”填写空白。
(1)空气中元素含量:氮_____氧;
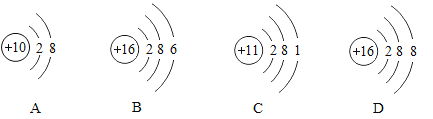
(2)核外电子数:钠离子_____钠原子;
(3) 含碳量:甲醛(CH2O)_____葡萄糖(C6HI2O6);
(4)物质在水中的溶解能力: Cu(OH)2_____CuSO4
(5)铜丝在火焰上灼烧,灼烧后的“铜丝”质量_____原铜丝 的质量;
(6)等质量金属与足量酸反应产生氢气的质量: Al_____ Mg。
【答案】> < = < > >
【解析】
(1)空气中元素含量氨气(78%),氧气(21%):氮>氧;
(2)核外电子数:钠离子失去一个电子为10电子,钠原子为10电子,钠离子<钠原子;
(3) 含碳量:甲醛(CH2O)含碳量=![]() ;葡萄糖(C6HI2O6)含碳量=
;葡萄糖(C6HI2O6)含碳量=![]() ;甲醛(CH2O)=葡萄糖(C6HI2O6);
;甲醛(CH2O)=葡萄糖(C6HI2O6);
(4)氢氧化铜是沉淀,不能溶于水,硫酸铜可以溶于水物质在水中的溶解能力: Cu(OH)2<CuSO4
(5)铜丝在火焰上灼烧,灼烧后与氧气反应生成氧化铜,“铜丝”质量>原铜丝 的质量;
(6)等质量金属与足量酸反应产生氢气的质量,由金属与酸反应关系,18g铝可以产生2g氢气,24g镁可以产生2g氢气,若等质量铝和镁分别与足量酸反应产生氢气的质量,
Al>Mg;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】化学兴趣小组的同学对某膨化食品包装袋内气体的成分进行探究,请你多与他们的探究,并回答下列问题.
[提出问题]包装袋内的气体成分是什么?
[猜想与假设]包装袋内的气体为猜想1:氧气;猜想2:氮气;猜想3:二氧化碳:猜想4:二氧化硫。
(1)通过分析,大家认为猜想1是错误的,理由是氧气化学性质比较活泼.食品易与氧气发生级慢氧化面变质;猜想4也是错误的,理由是________________。
[进行实验]为了探究气体的成分,甲.乙两位同学分别进行了如下实验。
[查阅资料]镁能在氮气中燃烧,反应生成氮化铁(Mg3N2)固体。氮化镁可与水剧烈反应产生氨气.该气体能使湿润的红色石蕊试纸变蓝。
(2)甲同学收集一.瓶该气体,把一根燃着的木条伸人瓶中,发现木条熄灭。由此得出气体是二氧化碳。乙同学认为该方案不可行.理由是_______________。
(3)为了验证剩余猜想,乙同学设计如下图所示方案
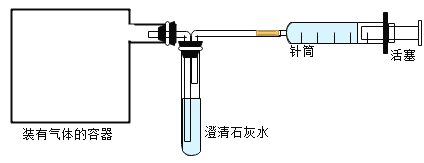
①在装有该气体的容器(容器内压强接近大气压强)上连接一个如图装置。向右拉动注射署活塞,经过实验后,发现澄清石灰水不变浑浊,证明猜想3不成立,猜想2.成立。
②为进一步确认猜想2成立,乙同学又进行了实验:
实验操作 | 实验现象 | 结论 |
a.另取一瓶气体,向其中伸入燃着的镁条,观察现象; b.取少量反应后固体于试管中。加入足量的蒸馏水然后______________________________观察现象 | a.镁条燃烧,发出耀眼白光;b红色的石蕊试纸___________。 | 猜想2成立 |
[交流讨论]
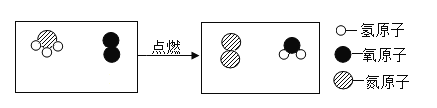
(4)试写出镁与氮气反应的化学方程式:_________________。
【题目】某些铜制品在空气中久置,表面生成绿色的铜锈(又称铜绿),主要成分是Cu2(OH)2CO3。某化学实验小组设计并进行实验,探究铜生锈的条件。
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
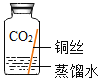
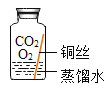
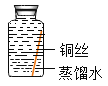
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
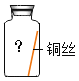
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____
(4)为验证猜想,请在下图中将实验⑤补充完整。__________
(5)结合上述实验,你对保存铜制品的建议是_____。
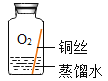
【题目】高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
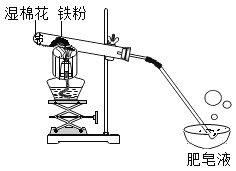
(1)试管尾部放一团湿棉花的目的是_____,
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_____。
(3)探究试管中剩余固体成分是什么?
[查阅资料]
几种常见铁的氧化物的颜色、状态及能否被磁铁吸引如下表所示。
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
Fe3O4能与稀硫酸反应而溶解,溶液变黄![]()
[初步验证]
试管中剩余固体为黑色,能全部被磁铁吸引,则剩余固体中一定不含氧化物_____。
[猜想与假设]
猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是_____。
实验操作 | 实验现象 | 结论 |
取少量黑色固体于试管中,滴加足量的稀硫酸 | _____, | 猜想一不成立,猜想二成立 |
[实验结论]铁和水蒸气反应的化学方程式为_____,