题目内容
【题目】常用燃烧法测定某些物质的组成。现取2.3g某物质在足量的氧气中完全燃烧,生成了4.4g CO2和2.7g H2O。对该物质的组成有下列推断:①一定含C、H元素 ②一定不含O元素 ③可能含O元素 ④一定含O元素 ⑤分子中C、H的原子个数比为2:5 ⑥分子中C、H的原子个数比为1:3 ⑦该物质中C、H、O的元素质量比为12:3:8 其中正确的是( )
A.①②⑥B.①④⑥⑦C.①③⑤D.①④⑤⑦
【答案】B
【解析】
由题意,反应后CO2和H2O生成,有机物一定含有C、H两种元素,则①正确;
CO2中C元素的质量4.4g×(![]() ×100%)=1.2g;H2O中H元素的质量2.7g×(
×100%)=1.2g;H2O中H元素的质量2.7g×(![]() ×100%)=0.3g,1.2g+0.3g=1.5g<2.3g,说明有氧元素,则④正确;
×100%)=0.3g,1.2g+0.3g=1.5g<2.3g,说明有氧元素,则④正确;
分子中C、H的原子个数比为![]() :
:![]() =1:3,则⑥正确;
=1:3,则⑥正确;
该物质中C、H、O元素的质量比为:1.2g:0.3g:(2.3-1.5)g=12:3:8,则⑦正确。故选B。

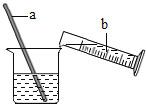
【题目】为验证“加热碳酸氢铵”所发生的变化和产物,两同学分别用甲、乙所示装置进行实验。
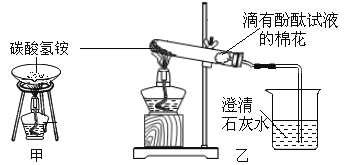
(1)甲实验中的现象是_______________。
(2)乙实验中试管口略向下倾斜的原因是_______________。乙实验中烧杯内反应化学方程式为_______________;实验中棉花逐渐变红色,则可说明反应产物中有_______________;相对于甲实验来说,乙实验的优点有(写一条)_______________。
(二)将一定量的K2CO3溶液与BaCl2溶液混合,过滤反应后的混合物。某兴趣小组的同学们欲探究滤液中溶质的组成。请你一同参与探究并回答有关问题:
[查阅资料]K2CO3溶液显碱性; BaCl2、 KCl溶液显中性。
[提出猜想]猜想1:滤液溶质是KCl;
猜想2:滤液溶质是_______________。
猜想3:滤液溶质是KCl和K2CO3。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
① 取少量滤液于试管中,滴几滴无色酚酞试液,振荡 | 无明显现象 | ①猜想_________不成立 |
② 另取少量滤液于另一支试管中,滴加K2CO3溶液 | ______________ | ②猜想2成立。 写出相关的化学方程式 _____________ |
[问题讨论]小丽同学认为要证明猜想2成立也可改用AgNO3溶液,你认为小丽同学不能达到实验目的,你的理由是_______________。
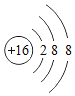
[反思拓展]实验结束后,组内同学认为K2CO3是盐而其水溶液却显碱性,这可能与它的构成微粒有关,微粒符号是_______________。