题目内容
【题目】某兴趣小组回收废旧锌锰电池制备皓矾晶体(ZnSO4·xH2O)。
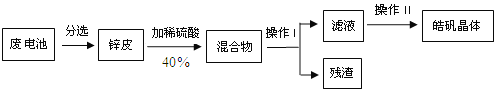
请回答下列问题:
(1)操作I为____________其中用到的玻璃棒作用是_______________________。
(2)写出锌皮加入稀硫酸发生反应的化学方程式_________________________。
(3)配制40%的稀硫酸的步骤有:①稀释 ②计算 ③装瓶并贴标签 ④量取,其正确的顺序为______(填序号)。配制过程中,需要的玻璃仪器有量筒、烧杯、玻璃棒及___________。
【答案】 过滤 引流 Zn+H2SO4=ZnSO4+H2↑ 2413 滴管
【解析】(1)操作Ⅰ是分离难溶性固体与液体的一种操作,是过滤,在过滤操作中玻璃棒的作用是引流;(2) 锌皮加入稀硫酸发生反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;(3)用浓硫酸配制40%的稀硫酸,先计算出所需浓硫酸和水的质量和体积,再量取浓硫酸和水的体积,然后进行溶解,最后进行装瓶并贴标签;需要用到烧杯、玻璃棒、量筒、胶头滴管等玻璃仪器。

 阅读快车系列答案
阅读快车系列答案【题目】在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5 mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
实验序号 | 滴加CuSO4 溶液的量 | 实验现象 |
① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多。振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式_____________。
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下稳定,70 ℃~80 ℃时分解生成氧化铜。
Ⅱ.铜酸钠[Na2Cu(OH)4]溶液呈亮蓝色。
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应。
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液。
甲同学认为猜想Ⅰ不成立,理由是______________________________。
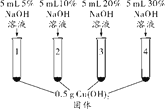
乙同学为验证猜想Ⅱ,进行了如下实验。
【进行实验】
实验操作 |
|
实验现象 | |
1号试管,…… | |
2号试管,蓝色固体不消失 | |
3号试管,蓝色固体减少 | |
4号试管,蓝色固体消失,得到亮蓝色溶液 |
【解释与结论】
(1)1号试管中现象为_________________________________。
(2)上述实验得出的结论是__________________________。
【反思与评价】
(1)进一步查阅资料可知,氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠,反应的化学方程式为__________________________。
(2)丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是____________________________。