题目内容
【题目】今有五种粒子的结构示意图,下列说法正确的是
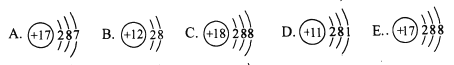
A. 它们表示四种元素 B. 它们都是原子
C. 它们都是离子 D. 它们都达到稳定结构
【答案】A
【解析】在原子结构示意图中,小圆圈表示原子核,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。最外层电子数决定原子的化学性质,A.质子数决定原子的类别,它们表示四种元素,正确;B. 同一原子中,质子数=核外电子数=核电荷数=原子序数;在阳离子中:质子数>核外电子;在阴离子中:质子数<核外电子;ACD都是原子;B为阳离子;E为阴离子;错误;C. BE是离子,ACD都是原子,错误; D. 原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构;BCE都达到稳定结构,错误;故选A。

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
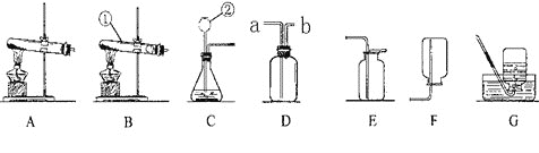
课堂练加测系列答案【题目】某研究小组用下图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。
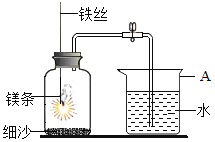
实验前,小组成员提出了不同的猜想。
【猜想与假设】
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,查阅资料知金属镁很活泼,可能会与空气中的氮气反应
【进行实验】
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的2/5 |
【解释与结论】
(1)Mg与氧气反应的化学方程式为_________。
(2)步骤Ⅰ说明装置的气密性_________。
(3)步骤Ⅱ中,关闭止水夹的目的是_________。
(4)推测猜想2成立的现象证据是_________。
【反思与评价】
(5)该小组认为,即使步骤Ⅲ中水的体积恰好占集气瓶体积的1/5,也不能说明猜想1成立,理由是_________。
(6)小组中同学对镁条与瓶中气体的反应提出了进一步的猜想:甲同学认为镁条先与O2反应,乙同学认为镁条先与N2反应。为进一步检验他们的猜想,可以进行的实验操作是:取少量镁条,点燃后迅速放入盛有空气的集气瓶中,待镁条熄灭后,________。
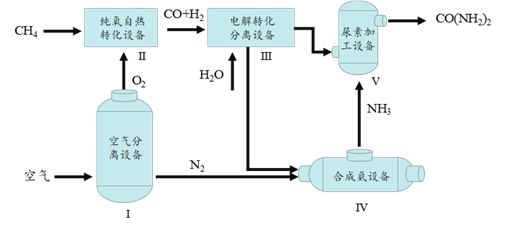
【题目】载人航天器工作舱中的空气要与地球上的空气基本一致。已知:在同温同压下,气体的体积之比等于分子个数之比。
(1)若用“![]() ”表示氮原子,“
”表示氮原子,“![]() ”表示氧原子,请在方框内用微观示意图表示工作舱中空气的主要成分。___________________。
”表示氧原子,请在方框内用微观示意图表示工作舱中空气的主要成分。___________________。
(2)宇航员呼出的CO2用氢氧化锂(LiOH)吸收,生成Li2CO3和H2O,反应的化学方程式为_______。
【答案】  CO2 + 2LiOH ==== Li2CO3 + H2O
CO2 + 2LiOH ==== Li2CO3 + H2O
【解析】本题考查了空气的成分等。
(1)空气中氮气和氧气应该均匀分布,且氮气与氧气的体积比约为4:1,用微观示意图表示工作舱中空气的主要成分,如图: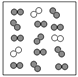
(2)宇航员呼出的CO2用氢氧化锂(LiOH)吸收,生成Li2CO3和H2O,反应的化学方程式为:CO2 + 2LiOH ==== Li2CO3 + H2O。
【题型】填空题
【结束】
20
【题目】阅读下面科普短文。
在中国古代化工发展的历史征程中,我国古代先民们在火药、制陶烧瓷、炼铜冶铁等化学加工技术方面取得了许多非凡的成就,为促进我国古代社会发展和人类的进步做出了重大的贡献。
【火药】人类最早使用的火药是黑火药,主要反应如下:

【制陶烧瓷】瓷器与陶器,都属于硅酸盐系列制品,最主要的化学成分是二氧化硅(SiO2)、氧化铝(Al2O3)及多种金属(Ca、Mg、Fe、K、Na等)氧化物。但在化学成分含量、用途等方面却大有区别。
制品 | 化学成分 | 性能用途等 |
陶器 | Al2O3 约15%~18%; Fe2O3约5%~6%; CaO、MgO等≥3%。 | 粗糙,不够坚硬,常用于取水、盛放食物等。 |
瓷器 | Al2O3 约18%~28%; Fe2O3约1%~2%; CaO、MgO等≤1%。 | 高温烧结,坚硬致密,洁白,薄, 呈半透明,敲击时清脆悦耳,美观,用途广泛,观赏、收藏价值高等。 |
【金属冶炼】制陶发展起来的高温技术为金属的冶炼、熔铸创造了条件,我国由新石器时代晚期逐步进入了先是炼铜(称为“青铜器时代”)后是炼铁(称为“铁器时代”)的金属时代。
青铜冶炼
天然铜夹杂在铜矿石之中,人们在加热熔化天然铜的过程中,将绿色的孔雀石[Cu2(OH)2CO3]、棕或黑色的锡石(SnO2)、蓝色的方铅矿(PbS)放在一起烧,便产生了青铜。青铜是铜与锡或铅熔成的合金。熔点比纯铜(1083℃)低100℃~300℃,更易加工和铸造,铸造性能也比纯铜好,硬度几乎提高一倍,适合制作工具和兵器。
铁的冶炼
到了春秋中后期,我国先民们在熟悉地掌握了块炼法炼铁后,又在世界上率先发明了以高温液体还原法冶炼生铁的技术,这在冶金史上是一个划时代的进步。
随着炼铁技术的进步,人们也逐渐懂得了炼钢。生铁和钢都是铁碳合金。含碳量>2%,为生铁;含碳量<0.02%,为纯铁;含碳量在两者之间为钢。依据文章内容回答下列问题。
(1)黑火药的主要成分是________。
(2)陶器与瓷器化学成分的主要区别是_________。
(3)生铁的碳含量______(填“高于”或“低于”)钢的碳含量。
(4)与纯金属相比,合金的优点可能是________。
【题目】阅读下面科普短文(原文有删改)
食盐
食盐是生活中常用的调味品,主要成分是氯化钠,在人体中有调节水分、维持酸碱平衡等生理作用。
资料一:食盐的加工
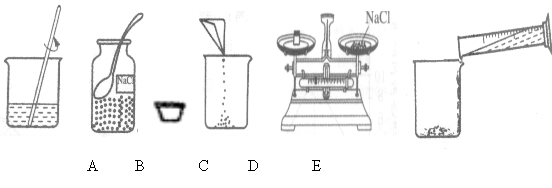
工业上用海水晒盐或用盐湖水、盐井水煮盐,使氯化钠晶体析出。这样制得的氯化钠含有较多的杂质,称为粗盐。粗盐经下图所示主要流程可成为精盐。

资料二:食盐的种类
市面上食盐制品种类繁多,现简要介绍几种。原盐,即粗盐,常用于腌制工艺;精盐,由粗盐提纯而成,适合烹饪调味;碘盐,在食盐中添加一定量碘酸钾(KIO3)即为碘盐,可防治碘缺乏病;低钠盐,食盐中添加氯化钾、硫酸镁等有“咸味”的成分,可防治因钠离子摄入过多而引起的高血压等疾病。
资料三:食盐的摄入量
虽然我们的身体离不开食盐,但摄入过多也会对身体产生危害。按照世界卫生组织的推荐标准,成人每天食盐摄入量不宜超过6g。然而据调查,我国人均每天的食盐摄入量为9.1g。一方面三餐中食盐量需要控制,另一方面,许多成品食物中食盐的含量也应引起重视,下表所示为部分成品食物每100g中的食盐含量。
食品 | 某品牌方便面 | 某品牌酱油 | 某品牌薯片 |
食盐含量g/100g | 3 | 16 | 1.6 |
依据文章内容回答下列问题。
(1)由粗盐制得精盐的过程属于_________(填“物理”或“化学”)变化。
(2)成人每天食盐摄入量不宜超过_____________g。
(3)如果某人一天吃了两袋(共300g)上表中所示方便面,按照世界卫生组织推荐标准,其当天食盐摄入量________(填“超标”或“未超标”)。
(4)下列关于食盐的说法正确的是_________。
A.高血压患者,可适当选择低钠盐
B.目前我国居民食盐摄入量普遍偏高
C.氯化钠是维持人体生命活动的重要物质
D.为补充人体所需钠元素和氯元素,每天做饭时可加入大量食盐
(5)请你为人们提一条日常摄取食盐的建议:_________________________。