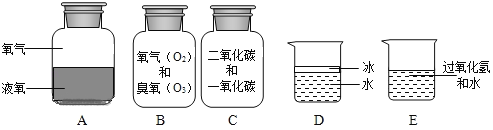
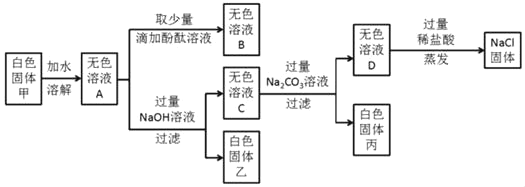
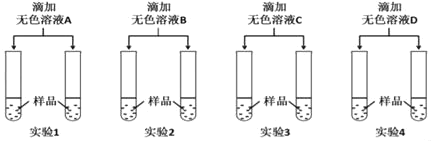
题目内容
【题目】18世纪末,法国科学家拉瓦锡重复了其他科学家的实验并做了相反的实验来揭秘水的组成。现在我们也可以在实验室用电解水的方法来验证水的组成。请回答下列问题:
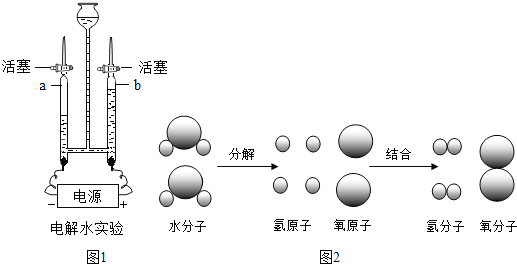
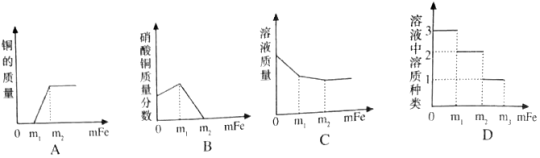
(1)图1为电解水的实验装置图。接通电源观察到两电极都有气泡产生。通电一段时间后,检验玻璃管b收集到的气体的方法是:打开b玻璃管处的活塞,将______。结合实验现象,写出电解水的化学方程式______。
(2)图2为水分解的微观过程:从图2中你能得出的结论是______。
(3)已知同温同压下,气体的体积比决定于气体的分子个数比。该实验中能够说明水的化学式为“H2O”的实验现象是______
【答案】将带火星的木条放在b导管口,木条复燃,该气体是氧气 2H2O![]() 2H2↑+O2↑ 化学变化的本质是分子破裂原子重组 负极(a管)产生的气体是正极(b管)的两倍
2H2↑+O2↑ 化学变化的本质是分子破裂原子重组 负极(a管)产生的气体是正极(b管)的两倍
【解析】
(1)通过观察图可以发现:a管气体多,且连着电源的负极,故a所收集的气体是氢气,b管气体少,且连着电源的正极,故b所收集的气体是氧气;
检验玻璃管b收集到的气体的方法是:打开b玻璃管处的活塞,将将带火星的木条放在b导管口,木条复燃,该气体是氧气;电解水时生成氧气和氢气,故水通电分解的化学方程式为2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
(2)在化学变化中,分子可以再分,而原子不可再分;
(3)根据同温同压下体积比等于分子个数比,实验生成氢气和氧气的体积比为2:1,故氢分子和氧分子的分子个数比为2:1,同时由于氢分子和氧分子都是双原子分子,所以可知水分子中氢原子和氧原子的个数比为2:1,水分子的化学式是H2O。
答案:
(1)将带火星的木条放在b导管口,木条复燃,该气体是氧气; 2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
(2)化学变化的本质是分子破裂原子重组(合理即可);
(3)负极(a管)产生的气体是正极(b管)的两倍

【题目】某兴趣小组话动中,同学们按图11装置对“可燃物燃烧的条件”进行探究。探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
【变流与讨论】白烟对人体健康有害,该实验装置必须改进。
【改进与实验】同学们按改进后的图12装置进行实验。
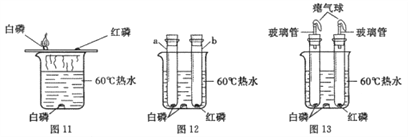
请你帮助他们将下表补充完整。
现象 | 解释 |
A a试管中白磷燃烧,热水中白磷没有燃烧. B b试管中红磷没有燃烧. | b试管中红磷、热水中白磷都没有燃烧的原因是①_______________________;②_______________________。 |
【反思与评价】 (1)改进后的图12装置与图11装置比较,优点是__________________。
(2)小林同学指出图12装置仍有不足之处,并设计了图13装置,其中气球的作用是___________。
【拓展与迁移】
实验小结时,小朱同学说:“待a试管冷却后,如果将试管口紧贴水面(室温下)。并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。
小晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测。
甲:接近试管容积的1/5; 乙:不一定接近试管容积的1/5。
你赞同的预测是_________(填“甲”或“乙”),理由是_________________________。
【题目】某同学按课本要求做CuSO4溶液与NaOH溶液反应的实验,有蓝色沉淀生成,对该沉淀进行加热,一般看到蓝色沉淀变黑色,可有时却看到蓝色沉淀变绿色。该同学对着异常现象产生了兴趣,决定对这现象产生的实验条件进行探究。
(查阅资料)难溶性碱受热易分解成对应的金属氧化物
写出上述生成蓝色沉淀以及蓝色沉淀变黑色的化学反应方程式:___________、__________。
(提出问题)加热蓝色沉淀没有出现黑色固体与什么因素有关?
(作出猜想)1.与CuSO4溶液过量有关;2.与NaOH溶液过量有关
(设计实验)限选试剂:1%的NaOH溶液,20%NaOH溶液,20%CuSO4溶液,1%CuSO4溶液
实验方案 | 实验现象 | 实验结论 |
1.往2mL20%CuSO4溶液中滴加2滴1%NaOH溶液,再将所得沉淀加热。 | 先产生蓝色沉淀,加热后 ______。 | 猜想1不成立 |
2._____,再将所得沉淀加热。 | 先产生蓝色沉淀,加热后 _______。 | 猜想2成立 |
(得到结论)在上述实验中,要能观察到蓝色沉淀变黑色,关键是___________
(拓展与反思)进一步查阅资料可知上述绿色物质是溶解度与氢氧化铜更小的水胆矾[化学式为Cu4(OH)6SO4],在碱性较强的条件下容易形成,继续加热一段时间该绿色固体则可产生黑色沉淀,写出该反应方程式__________.