题目内容
【题目】学习金属单元后,小强知道了铁是当今世界用量最多的金属,而每年全世界被腐蚀损耗的钢铁材料,约占全年钢铁产量的十分之一。于是小强对金属铁的相关知识开展了探究性学习。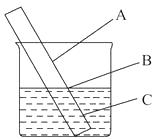
(1)如图,小强将一根长20 cm的光亮的铁棒放在自来水中,观察A、B、C三处的变化。几天后,他发现(填序号)处最先出现铁锈,小强结合书本知识知道,铁生锈实际是铁和、等物质发生反应的过程。
(2)小强来到已停产的企业厂房,看到许多机械设备上已锈迹斑斑,他马上想到可以用稀盐酸将铁锈(主要成分Fe2O3)除去,该反应的化学方程式为:。去锈后为防止机械设备进一步锈蚀,小强想到的一种防护方法是。
【答案】
(1)B;氧气;水(或者O2 H2O)
(2)Fe2O3+6HCl=2FeCl3+3H2O;涂油(或刷漆等合理即可)
【解析】铁制品在与空气、水共存的条件下更容易生锈,所以图中金属铁在B点更容易生锈;稀盐酸与氧化铁反应生成氯化铁和水;防止金属生锈的方法有很多,如涂油、刷漆、制成不锈钢等。
故答案为:(1)B;氧气;水(或者O2 H2O)(2)Fe2O3+6HCl=2FeCl3+3H2O;涂油(或刷漆等合理即可)(1)铁生锈的条件是与水和氧气接触
(2)氧化铁和盐酸反应生成氯化铁和水,铁锈消失,金属在水和氧气共同作用下生锈,因此隔绝其中一项即可防锈

【题目】工业上采用氨碱法生产纯碱,主要流程如下图,请据图回答相关问题。![]()
(1)氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显色。
(2)从步骤①提取粗盐常用(填“蒸发结晶”或“降温结晶”)方法。
(3)从酸碱反应的角度分析,步骤④中通入氨气的作用是。
(4)步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途。
(5)步骤⑥中发生反应的化学方程式为 , 该反应类型属于反应。
(6)工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
时间/s | 0 | 5 | 10 | 15 |
读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
请你据此分析计算:
①实验中产生二氧化碳的质量为;
②该产品中碳酸钠的质量分数 (写出计算过程,结果精确到0.1%)
