题目内容
某二价金属M的氧化物10 g与90 g稀硫酸恰好完全反应后,形成无色透明溶液,测得反应后溶液中溶质的质量分数为30% 。请计算(保留一位小数):
(1)该金属M的相对原子质量和上述稀硫酸中溶质的质量分数。
(2)反应后的溶液中,氢元素与氧元素的质量比。
(1)反应后的溶液中溶质质量为:(10g+90g)×30%  == 30g
== 30g
设金属M的相对原子质量为m,稀硫酸中H2SO4的质量为x
MO + H2SO4 == MSO4 + H2O
m+16 98 m+96
10g x 30g
(m+16) :(m+96)== 10g :30g
解得m == 24 可知M为镁元素------------- (1分,不判断是镁不扣分)
98 :x ==(m+96) :30g 解得x == 24.5g
ω(H2SO4) == (24.5g÷90g)×100% == 27.2%------------- (1分)
(2)已知反应后的溶液中MgSO4的质量分数为30%,则H2O为70%
即m (H2O) :m (MgSO4) == 70 :30 == 7 :3
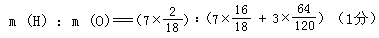
== 35 :352

练习册系列答案
相关题目