题目内容
【题目】CO2通入NaOH溶液中没有明显现象,CO2与NaOH溶液是否发生了化学反应呢?某化学兴趣小组的同学对此进行了如下探究。
(查阅资料)
①通常情况下,1体积的水溶解1体积的CO2.②碳酸钡是种难溶于水的白色固体。
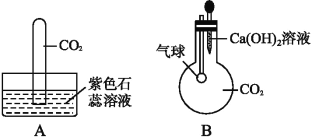
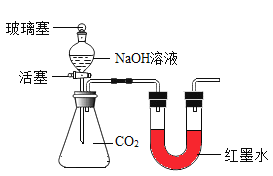
(实验探究)小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并利用该装置进行实验,打开玻璃塞和活塞,使NaOH溶液快速滴入锥形瓶中,再立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管右侧的红墨水液面_____(选填“升高“降低”或“不移动”)。小红同学根据此现象判断出CO2和NaOH溶液发生了反应,理由是_____。
(反思与评价)小明同学认为小红同学的实验方案不严密,理由是_____。
(拓展实验)该兴趣小组的同学为此又设计了下表所示的两种实验方案做进一步的探究,请完成下列表格。
实验序号 | 实验方案 | 实验现象 | 结论 |
方案一 | 向通有二氧化碳的氢氧化钠溶液中滴加过量的_____(填试剂名称) | 最终有气泡产生 | CO2与NaOH溶液发生了反应,反应的化学方程式为_____ |
方案二 | 向通有二氧化碳的氢氧化钠溶液中滴加氢氧化钡溶液 | _____ |
【答案】降低 U型管内右侧液面下降,说明锥形瓶内的压强减小,从而说明氢氧化钠与二氧化碳发生了反应 二氧化碳溶于水也会使锥形瓶内的压强变小 稀盐酸 2NaOH+CO2=NaCO3+H2O 有白色沉淀产生
【解析】
实验探究:
氢氧化钠与二氧化碳反应会导致锥形瓶内的压强变小,在大气压的作用下会观察到U型管右侧的红墨水液面下降,根据此现象判断出CO2和NaOH溶液发生了反应,理由是U型管内右侧液面下降,说明锥形瓶内的压强减小,从而说明氢氧化钠与二氧化碳发生了反应;
反思与评价:二氧化碳溶于水也会使锥形瓶内的压强变小,故该实验存在一定的缺陷;
拓展实验:碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳气体,碳酸钠能与氢氧化钡反应生成碳酸钡白色沉淀和氢氧化钠 。因此:
实验序号 | 实验方案 | 实验现象 | 结论 |
方案一 | 向通有二氧化碳的氢氧化钠溶液中滴加过量的 稀盐酸 | 最终有气泡产生 | CO2与NaOH溶液发生了反应,反应的化学方程式为 2NaOH+CO2=NaCO3+H2O |
方案二 | 向通有二氧化碳的氢氧化钠溶液中滴加氢氧化钡溶液 | 有白色沉淀产生 |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案